题目内容
11.下列各组有机物中,其一氯代物的数目不相等的是( )(1)正戊烷和正己烷
(2)苯和乙烷
(3)对二甲苯和2,2-二甲基丙烷
(4)甲苯和2-甲基丙烷.
| A. | (2)(4) | B. | (3)(4) | C. | (1)(3) | D. | (1)(2) |
分析 烷烃的一氯代物种类,取决于有机物分子中氢原子的种类,先根据有机物名称判断有机物中氢原子种类,然后判断一氯代物种类,比较选项中的有机物一氯代物是否相等即可.
解答 A、戊烷分子中氢原子有3种,一氯代物有3种;正己烷分子中氢原子3种,一氯代物有3种,所以二者一氯代物数目相同,故A错误;
B、苯分子中氢原子只有1种,一氯代物只有1种;乙烷分子中的氢原子有1种,一氯代物只有1种,二者一氯代物数目相同,故B错误;
C、对二甲苯分子中氢原子有2种,一氯代物有2种;2,2-二甲基丙烷分子中氢原子有1种,一氯代物只有一种,二者一氯代物数目不同,故C正确;
D、甲苯分子中氢原子有4种,一氯代物有4种,2-甲基丙烷分子氢原子有2种,一氯代物有2种,二者一氯代物都有2种,故D正确;
故选B.
点评 本题考查了有机物的同分异构体数目计算,可以根据烃中的氢原子种类,确定取代产物种类,本题难度中等.

练习册系列答案
相关题目
1.下列有关描述中正确的是( )
| A. | 常温下硝酸铵溶于水是一个能自发进行的吸热过程,说明该过程的△S>0 | |
| B. | 反应 A(g)+3B(g)?2C(g)达平衡后,升高温度,平衡常数增大,则正反应的△H<0 | |
| C. | 已知H+(aq)+OH- (aq)=H2O(l);△H=-57.3 kJ/mol.将4 g氢氧化钠固体放入100 mL 1 mol/L的稀盐酸中,放出了5.73 kJ的热量 | |
| D. | 检验C2H5Cl中的氯元素:先将C2H5Cl与NaOH溶液混合后加热,冷却后再AgNO3溶液 |
19.乙酸与乙酸乙酯的混合物中H元素的质量分数是$\frac{1}{11}$,则O元素的质量分数是( )
| A. | $\frac{10}{11}$ | B. | $\frac{7}{11}$ | C. | $\frac{6}{11}$ | D. | $\frac{4}{11}$ |
3.X、Y为同周期元素,如果X的原子半径大于Y,则下列说法不正确的是( )
| A. | 若X、Y均为金属元素,则X的金属性强于Y | |
| B. | 若X、Y均为金属元素,则X的阳离子氧化性比Y的阳离子氧化性强 | |
| C. | 若X、Y均为非金属元素,则Y的气态氢化物比X的稳定 | |
| D. | 若X、Y均为非金属元素,则最高价氧化物所对应的水化物的酸性Y强于X |
20.下列关于粒子结构的描述不正确的是( )
| A. | H2S和NH3价电子总数均是8 | |
| B. | 次氯酸分子的结构式为:H-Cl-O | |
| C. | HS-和HCl均是含一个极性键的18电子粒子 | |
| D. | 1 mol D216O中含中子、质子、电子各10 NA(NA代表阿伏加德罗常数的值) |
1.下列各选项中所述的两个量,前者一定大于后者的是( )
| A. | pH=10的NaOH和CH3COONa溶液中,水的电离程度 | |
| B. | 25℃与80℃纯水的pH | |
| C. | 将pH=3的醋酸和盐酸分别稀释100倍后溶液的pH | |
| D. | 相同温度下,10mL0.1mol•L-1的醋酸与100mL0.01mol•L-1的醋酸中的H+物质的量 |
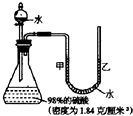 如图所示的装置,打开分液漏斗的活塞,让水滴入锥形瓶中可以看到水浮在硫酸上面且水立即沸腾,硫酸液滴飞溅,同时U形管中甲端下降,乙端上升.这个实验说明了浓硫酸的密度大于水的密度、浓硫酸溶于水的时候放出热量,这个事实告诉我们为了防止发生事故,在稀释浓硫酸时,一定要将浓硫酸沿容器壁慢慢倒入水中,并不断搅拌.
如图所示的装置,打开分液漏斗的活塞,让水滴入锥形瓶中可以看到水浮在硫酸上面且水立即沸腾,硫酸液滴飞溅,同时U形管中甲端下降,乙端上升.这个实验说明了浓硫酸的密度大于水的密度、浓硫酸溶于水的时候放出热量,这个事实告诉我们为了防止发生事故,在稀释浓硫酸时,一定要将浓硫酸沿容器壁慢慢倒入水中,并不断搅拌.
 ;
; ;
;