题目内容
阿伏加德罗常数约为6.02×1023mol-1,下列说法中一定正确的是
| A.1 L 1 mol?L-1的HAc溶液中含有氢离子数约为6.02×1023 |
| B.18 g D2O(重水)完全电解,转移的电子数约为6.02×1023 |
| C.标态下,22.4L NO2气体,所含氧原子数约为2×6.02×1023 |
| D.标态下,14g乙烯和丙烯的混合物中,含有共用电子对数目约为3×6.02×1023 |
D
解析试题分析:A、醋酸是弱酸存在电离平衡,因此1L 1mol?L-1的HAc溶液中含有氢离子数小于6.02×1023,故A错误;B、18g D2O(重水)物质的量=18g÷20g/mol=0.9mol。重水完全电解,则根据方程式2D2O→2D2+O2可知,转移的电子数约为0.9×2×6.02×1023,故B错误;C、二氧化氮和四氧化二氮间存在化学平衡2NO2 N2O4,标态下,22.4L NO2气体物质的量为1mol,所含氧原子数大于2×6.02×1023,小于4×6.02×1023,故C错误;D、乙烯和丙烯的最简式均是CH2,所以14g乙烯和丙烯的混合物中,含有共用电子对数目约为
N2O4,标态下,22.4L NO2气体物质的量为1mol,所含氧原子数大于2×6.02×1023,小于4×6.02×1023,故C错误;D、乙烯和丙烯的最简式均是CH2,所以14g乙烯和丙烯的混合物中,含有共用电子对数目约为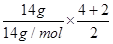 ×6.02×1023=3×6.02×1023,故D正确,答案选D。
×6.02×1023=3×6.02×1023,故D正确,答案选D。
考点:考查阿伏加德罗常数的有关计算和判断

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.24g NaH中阴离子所含电子总数为NA |
| B.标准状况下,22.4 L苯中含有C—H键数目为6NA |
| C.在碳酸钠溶液中,若c(CO32-)="1" mol?L-1,则c(Na+)="2" mol?L-1 |
| D.通过MnO2催化使H2O2分解,产生32gO2时转移电子数为2NA |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,33.6L氟气中含有氟原子的数目为1.5NA |
| B.28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA |
| C.常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA |
| D.50mL18.4mol·L-1浓硫酸与足量铜加热反应,生成SO2分子的数目为0.46NA |
下列化学表述正确的是
A.氯化钠的晶体模型: |
B.铍原子最外层的电子云图: |
| C.次氯酸的结构式:H-O-Cl |
| D.CH3CHOHCH(CH3)2名称:2-3-二甲基丙醇 |
下列微粒中,对水的电离平衡不产生影响的是
A. | B.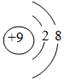 | C.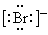 | D.1s22s22p63s1 |
将78 g金属钾在空气中燃烧,生成KO2和K2O2的混合物。该混合物与足量的CO2充分反应后生成O2(4KO2+2CO2→2K2CO3+3O2),得到O2的物质的量可能为
| A.0.50 mol | B.0.75 mol | C.1.00 mol | D.1.50 mol |
用NA表示阿伏加德罗常数,下列叙述正确的是
| A.46 g乙醇中含有的化学键数为7 NA |
| B.1 mol氯气和足量NaOH溶液反应转移电子数为2 NA |
| C.1 mol OH-和1 mol -OH(羟基)中含有的质子数均为 9 NA |
| D.10 L 0.1 mol·L-1的Na2CO3溶液中,Na+、CO2- 3总数为3 NA |
用NA表示阿伏加德罗常数,下列叙述中,正确的是
| A.常温常压下,5.6 g N2和CO混合物中所含有的原子总数为0.4NA |
| B.0.1 molNa2 O2中所含的阴离子数为0.2NA |
| C.将0.2 molFeCl3水解制成胶体,所得胶体粒子数为0.2 NA |
| D.标准状况下,2.24 L H2O中含有的氧原子数目为0.1 NA |