题目内容
8.下列实验中所选用的仪器或者所测数据合理的是( )| A. | 用精密pH试纸测定血液的pH为7.40 | |
| B. | 用碱式滴定管量取20.10mLKMnO4酸性溶液 | |
| C. | 用托盘天平称取8.56g食盐 | |
| D. | 用250mL容量瓶配制所需的230mL0.2 mol•L-1的氢氧化钠溶液 |
分析 A.精密pH试纸能精确到0.1;
B.高锰酸钾具有氧化性,腐蚀橡皮管;
C.托盘天平能准确到0.1g;
D.根据容量瓶的使用规则进行解答.
解答 解:A.精密pH试纸能精确到0.1,无法测得pH为7.40,故A错误;
B.高锰酸钾具有氧化性,腐蚀橡皮管,应用酸式滴定管,故B错误;
C.托盘天平能准确到0.1g,用托盘天平不能称取8.56g食盐,故C错误;
D.先用250mL容量瓶能配制250mL0.2mol/L的氢氧化钠溶液,然后取230mL0.2 mol•L-1的氢氧化钠溶液即可,故D正确.
故选D.
点评 本题考查实验仪器的使用和注意事项,题目难度不大,注意基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.甲溶液PH是1,乙溶液PH是2,甲溶液与乙溶液的氢离子浓度之比为( )
| A. | 10﹕1 | B. | 1﹕10 | C. | 2﹕1 | D. | 1﹕2 |
3.已知胆矾溶于水时溶液温度降低,室温下将1mol无水硫酸铜制成溶液时放出热量为Q1kJ,又知胆矾分解的热化学方程式为CuSO4•5H2O(s)═CuSO4(s)+5H2O(l);△H=+Q2 kJ•mol?1则Q1、Q2的关系为( )
| A. | Q1>Q2 | B. | Q1<Q2 | C. | Q1=Q2 | D. | 无法确定 |
13.已知:HA(aq)+OH-(aq)═A-(aq)+H2O(l)△H=-12.1kJ•mol-1;H+(aq)+OH-(aq)═H2O(l)△H=-55.6kJ•mol-1.则HA在水溶液中的电离反应HA(aq)?H+(aq)+A-(aq)的△H等于( )
| A. | -67.7 kJ•mol-1 | B. | -43.5 kJ•mol-1 | C. | +43.5 kJ•mol-1 | D. | +67.7 kJ•mol-1 |
17.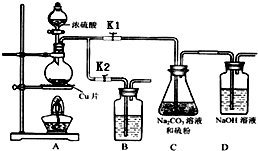 硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.
已知:①Na2S2O3在酸性溶液中不能稳定存在;
②硫代硫酸钠与碘反应的离子方程式为:2S2O32-+I2→S4O62-+2I-.
(Ⅰ)制备Na2S2O3•5H2O
①打开K1,关闭K2,向放有铜片的圆底烧瓶中加入足量浓硫酸,加热.圆底烧瓶中发生反应的化学方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
②C中混合液被气流搅动,反应一段时间后,
硫粉的量逐渐减少.
C中碳酸钠的作用是提供碱性环境,作反应物.
D中可能发生的离子反应方程式为:SO2+2OH-=SO32-+H2O、CO2+2OH-=CO32-+H2O.
“停止C中的反应”的操作是打开K2,关闭K1.
③过滤C中的混合液.将滤液加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品.
④装置B中盛放的试剂是(填化学式)NaOH溶液,其作用是在C中的反应停止后,吸收A中产生的多余SO2,防止空气污染.
(Ⅱ)用I2的标准溶液测定产品的纯度
取5.5g产品,配制成100mL溶液.取10.00mL溶液,以淀粉溶液为指示剂,用浓度为0.050mol/L I2的标准溶液进行滴定,相关数据记录如下表所示.
(1)滴定时,达到滴定终点的现象是加入最后一滴I2标准溶液后,溶液变蓝,且半分钟内颜色不改变.
(2)Na2S2O3•5H2O在产品中的质量分数是90.2%(用百分数表示,且保留1位小数).
 硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.已知:①Na2S2O3在酸性溶液中不能稳定存在;
②硫代硫酸钠与碘反应的离子方程式为:2S2O32-+I2→S4O62-+2I-.
(Ⅰ)制备Na2S2O3•5H2O
①打开K1,关闭K2,向放有铜片的圆底烧瓶中加入足量浓硫酸,加热.圆底烧瓶中发生反应的化学方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
②C中混合液被气流搅动,反应一段时间后,
硫粉的量逐渐减少.
C中碳酸钠的作用是提供碱性环境,作反应物.
D中可能发生的离子反应方程式为:SO2+2OH-=SO32-+H2O、CO2+2OH-=CO32-+H2O.
“停止C中的反应”的操作是打开K2,关闭K1.
③过滤C中的混合液.将滤液加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品.
④装置B中盛放的试剂是(填化学式)NaOH溶液,其作用是在C中的反应停止后,吸收A中产生的多余SO2,防止空气污染.
(Ⅱ)用I2的标准溶液测定产品的纯度
取5.5g产品,配制成100mL溶液.取10.00mL溶液,以淀粉溶液为指示剂,用浓度为0.050mol/L I2的标准溶液进行滴定,相关数据记录如下表所示.
| 编号 | 1 | 2 | 3 |
| 溶液的体积/mL | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.95 | 17.10 | 20.05 |
(2)Na2S2O3•5H2O在产品中的质量分数是90.2%(用百分数表示,且保留1位小数).
