题目内容
在常温下,向20L密闭容器中通入a mol H2、b mol O2(a≤4,b≤4,A.b均为正整数),点燃后充分反应恢复至原温度时,容器内气体(水蒸气忽略不计)密度最大值可能是( )
A.5.6 g·L-1 B.9.6 g·L-1 C.11.2g·L-1 D.56 g·L-1
A.5.6 g·L-1 B.9.6 g·L-1 C.11.2g·L-1 D.56 g·L-1
A
试题分析:发生反应2H2+O2
 2H2O,如果有气体剩余,则密闭容器中气体有一定的密度.如果两者恰好反应完全,则气体密度约为0.剩余气体密度最大,由于氧气的相对分子质量大于氢气,故应该使氧气最多而氢气最少,剩余氧气即可,
2H2O,如果有气体剩余,则密闭容器中气体有一定的密度.如果两者恰好反应完全,则气体密度约为0.剩余气体密度最大,由于氧气的相对分子质量大于氢气,故应该使氧气最多而氢气最少,剩余氧气即可,2H2 + O2
 2H2O,
2H2O,amol 0.5amol,
故剩余氧气为(b-0.5a)mol,
故剩余气体的密度为〔(b?0.5a)mol×32g/mol〕/20L=1.6(b-0.5a)g/mol,由于a≤4,b≤4,A.b均为正整数,故b=4,a=1时,剩余气体密度最大为1.6(4-0.5×1)g/mol=5.6g/mol,

练习册系列答案
相关题目
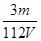 mol·L-1
mol·L-1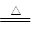 Cu3P2+3H2而增重4.96 g;第二支玻璃管反应后质量减轻了5.76 g。
Cu3P2+3H2而增重4.96 g;第二支玻璃管反应后质量减轻了5.76 g。 2SO3(g) 和4SO2(g)+2O2(g)
2SO3(g) 和4SO2(g)+2O2(g) CO2+2H2O+4Cu。当CH4完全反应后,硬质玻璃管的质量减轻4.8克。将该反应后产生的气体通过过量澄清石灰水中,充分吸收,生成沉淀8.5克。
CO2+2H2O+4Cu。当CH4完全反应后,硬质玻璃管的质量减轻4.8克。将该反应后产生的气体通过过量澄清石灰水中,充分吸收,生成沉淀8.5克。