题目内容
对于给定的可逆反应的平衡常数(K)的说法正确的是( )
| A.K只与温度有关,温度不变,K不变 |
| B.改变条件,反应物的转化率增大,K也一定增大 |
| C.温度一定时,其正、逆反应的K相等 |
| D.若正反应△H<0,升高温度,该反应的K增大 |
A.平衡常数指各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,只与温度有关,故A正确;
B.改变条件,化学平衡可能向正反应方向移动,则反应物的转化率增大,K增大;也可能向逆反应方向移动,则反应物转化率降低,K减小,故B错误;
C.温度相同时,正逆反应方向的反应物和生成物正好反过来,则K表达式不同,且互为倒数,故C错误;
D.正反应△H<0,放热,升高温度向逆反应方向移动,则生成物浓度降低,反应物浓度增大,故D错误;
故选A.
B.改变条件,化学平衡可能向正反应方向移动,则反应物的转化率增大,K增大;也可能向逆反应方向移动,则反应物转化率降低,K减小,故B错误;
C.温度相同时,正逆反应方向的反应物和生成物正好反过来,则K表达式不同,且互为倒数,故C错误;
D.正反应△H<0,放热,升高温度向逆反应方向移动,则生成物浓度降低,反应物浓度增大,故D错误;
故选A.

练习册系列答案
相关题目

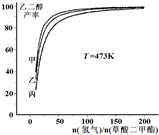 (氢气)/n(草酸二甲酯)]和压强的变化关系,其中三条曲线分别表示体系压强为1.5MPa、2.5MPa、3.5MPa的情况,则曲线甲对应的压强是P(甲)=______.
(氢气)/n(草酸二甲酯)]和压强的变化关系,其中三条曲线分别表示体系压强为1.5MPa、2.5MPa、3.5MPa的情况,则曲线甲对应的压强是P(甲)=______.