题目内容
利用下列实验装置能完成相应实验的是
- A.装置①测定化学反应速率
- B.装置②制取并吸收HCl
- C.装置③制备纯净的NH3
- D.装置④模拟铁的腐蚀
AD
分析:A.可根据一定时间内生成气体的体积测定反应速率;
B.导管不能插入液面以下;
C.氨气不能用氯化钙干燥;
D.根据铁的腐蚀类型以及原理分析.
解答:解:A.根据一定时间内生成气体的体积,可测定化学反应速率,故A正确;
B.装置②可制取HCl,但尾气吸收装置不能将导管插入液面以下,会发生倒吸,故B错误;
C.装置③可用碱性干燥剂吸收水和二氧化碳,氯化钙和氨气能发生络合反应,不能用氯化钙干燥,故C错误;
D.在食盐水中铁发生吸氧腐蚀,在醋酸中发生析氢腐蚀,U形管内左端红墨水上升,右端红墨水下降,故D正确.
故选AD.
点评:本题考查化学实验方案的评价,题目难度不大,易错点为C,注意氯化钙作为干燥剂的性质.
分析:A.可根据一定时间内生成气体的体积测定反应速率;
B.导管不能插入液面以下;
C.氨气不能用氯化钙干燥;
D.根据铁的腐蚀类型以及原理分析.
解答:解:A.根据一定时间内生成气体的体积,可测定化学反应速率,故A正确;
B.装置②可制取HCl,但尾气吸收装置不能将导管插入液面以下,会发生倒吸,故B错误;
C.装置③可用碱性干燥剂吸收水和二氧化碳,氯化钙和氨气能发生络合反应,不能用氯化钙干燥,故C错误;
D.在食盐水中铁发生吸氧腐蚀,在醋酸中发生析氢腐蚀,U形管内左端红墨水上升,右端红墨水下降,故D正确.
故选AD.
点评:本题考查化学实验方案的评价,题目难度不大,易错点为C,注意氯化钙作为干燥剂的性质.

练习册系列答案
相关题目
Ⅰ.某研究性学习小组用10g胆矾制取CuO,并证明CuO可以催化H2O2的分解反应.
(1)首先制备CuO,实验步骤如下,请完成缺少的步骤:
①称取10g胆矾,放入小烧杯中,再加水溶解;②向小烧杯中滴加NaOH溶液,至产生大量沉淀;③用酒精灯在石棉网上加热小烧杯,至沉淀物完全黑色;④将以上混合物过滤,洗涤,______,然后研细;⑤检查④中洗涤是否完全的操作是______.
(2)用图1所示,按表中设计实验方法,证明CuO能催化7%H2O2溶液的分解,并与MnO2的催化效果进行比较.
| 实验序号 | 双氧水体积 | 催化剂 | 待测数据 |
| a | 15mL | 无 | |
| b | 15mL | 0.5g CuO | |
| c | 15mL | 0.5g MnO2 |
②为探究CuO在实验b中是否起催化作用,除与
a比较外,还应补充以下实验(不必写具体操作):
A.证明CuO化学性质在反应前后是否改变;
B.______.
Ⅱ.摩尔盐[(NH4)2SO4?FeSO4?6H2O]
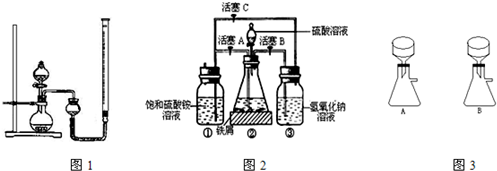
在空气中比一般亚铁盐稳定,是化学分析中常用的还原剂.某研究性学习小组用图2所示的实验装置来制取摩尔盐,实验步骤如下,回答下列问题:
(1)用30%的NaOH溶液和废铁屑(含少量油污、铁锈、FeS等)混合、煮沸、冷却、分离,将分离出的NaOH溶液装入③中.
(2)利用容器②的反应,向容器①中通入氢气,应关闭活塞______,打开活塞______(填字母).向容器①中通人氢气的目的是______.
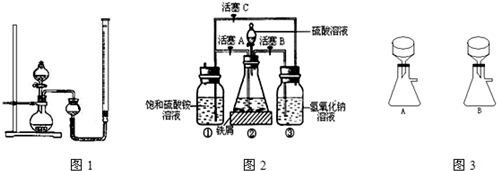
(3)待锥形瓶中的铁屑快反应完时,关闭活塞B、C,打开活塞A,继续产生的氢气会将锥形瓶中的硫酸亚铁(含极少部分未反应的稀硫酸)压到饱和硫酸铵溶液的底部.在常温下放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵,抽滤,制得硫酸亚铁铵晶体.图3是抽滤装置的一部分,其中正确的是______.(填A或B)
(4)为了确定产品中亚铁离子的含量,研究小组用滴定法来测定.若取产品24.50g配成100mL溶液,取出10.00mL用0.1000mol?L-1KMnO4酸性溶液滴定,消耗KMnO4溶液10.00mL.
已知高锰酸钾与Fe2+的离子方程式为:MnO
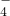 +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O试求产品中摩尔盐的质量分数______.(NH4)2SO4?FeSO4?6H2O的相对分子质量为392.
测定乙醇分子结构是经典的定量实验之一,反应原理为:乙醇+钠( 足量 ) →乙醇钠+氢气
选用图中所列仪器和导管组装实验装置。
序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
导 管 及 仪 器 |
|
|
|
|
|
|
|
每个橡皮塞上都打了两个孔 | |||||||
(1)气体发生器置于左侧,气体向右方流动,所用仪器与导管依次连接序号为6接______接______接______接______接______。
(2)进行实验时的操作如下(每项进行一次):
①从分液漏斗中逐滴把无水酒精加入烧瓶中,并控制反应速率,酒精加完后关闭活塞;
②在广口瓶中注入适量的水;
③待烧瓶冷却到室温后对量筒读数;
④把定量的V mL酒精无损地倒入分液漏斗中;
⑤检查装置的气密性;
⑥预先将小钠块在二甲苯中熔化成小钠珠,冷却后倒入烧瓶中,塞紧橡皮塞;
⑦估计反应接近完成,用酒精灯对烧瓶略加微热,使反应完成,再撤掉酒精灯。
正确的操作序号是______。
(3)①利用96%的乙醇制无水酒精的方法是 ________________________。
②将小钠块制成小钠珠的目的是 _______________________________。
(4)出现下列情况时,对实验结果的影响怎样?(A. 偏高 B. 偏低 C. 无影响 )
①此反应是放热反应,反应速率太快,使实验结果________________。
②如果无水酒精中混有少量甲醇,使实验结果____________________。
③读数时,如果量筒内的液面高于广口瓶内的液面,使实验结果__________。
(5)如果此实验的数据视作标准状况下的数据,无水乙醇的密度为ρg·cm-3, V mL乙醇反应完全后,量筒内的液面读数为m mL,则乙醇分子中能被取代的氢原子数是________ 。
Ⅰ.某研究性学习小组用10g胆矾制取CuO,并证明CuO可以催化H2O2的分解反应.
(1)首先制备CuO,实验步骤如下,请完成缺少的步骤:
①称取10g胆矾,放入小烧杯中,再加水溶解;②向小烧杯中滴加NaOH溶液,至产生大量沉淀;③用酒精灯在石棉网上加热小烧杯,至沉淀物完全黑色;④将以上混合物过滤,洗涤, ,然后研细;⑤检查④中洗涤是否完全的操作是 .
(2)用图1所示,按表中设计实验方法,证明CuO能催化7%H2O2溶液的分解,并与MnO2的催化效果进行比较.
①从设计原理看,实验中的待测数据是 .
②为探究CuO在实验b中是否起催化作用,除与
a比较外,还应补充以下实验(不必写具体操作):
A.证明CuO化学性质在反应前后是否改变;
B. .
Ⅱ.摩尔盐[(NH4)2SO4?FeSO4?6H2O]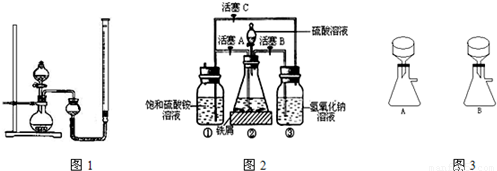
在空气中比一般亚铁盐稳定,是化学分析中常用的还原剂.某研究性学习小组用图2所示的实验装置来制取摩尔盐,实验步骤如下,回答下列问题:
(1)用30%的NaOH溶液和废铁屑(含少量油污、铁锈、FeS等)混合、煮沸、冷却、分离,将分离出的NaOH溶液装入③中.
(2)利用容器②的反应,向容器①中通入氢气,应关闭活塞 ,打开活塞 (填字母).向容器①中通入氢气的目的是 .
(3)待锥形瓶中的铁屑快反应完时,关闭活塞B、C,打开活塞A,继续产生的氢气会将锥形瓶中的硫酸亚铁(含极少部分未反应的稀硫酸)压到饱和硫酸铵溶液的底部.在常温下放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵,抽滤,制得硫酸亚铁铵晶体.图3是抽滤装置的一部分,其中正确的是 .(填A或B)
(4)为了确定产品中亚铁离子的含量,研究小组用滴定法来测定.若取产品24.50g配成100mL溶液,取出10.00mL用0.1000mol?L-1KMnO4酸性溶液滴定,消耗KMnO4溶液10.00mL.
已知高锰酸钾与Fe2+的离子方程式为:MnO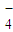 +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O
试求产品中摩尔盐的质量分数 .(NH4)2SO4?FeSO4?6H2O的相对分子质量为392.
(1)首先制备CuO,实验步骤如下,请完成缺少的步骤:
①称取10g胆矾,放入小烧杯中,再加水溶解;②向小烧杯中滴加NaOH溶液,至产生大量沉淀;③用酒精灯在石棉网上加热小烧杯,至沉淀物完全黑色;④将以上混合物过滤,洗涤, ,然后研细;⑤检查④中洗涤是否完全的操作是 .
(2)用图1所示,按表中设计实验方法,证明CuO能催化7%H2O2溶液的分解,并与MnO2的催化效果进行比较.
| 实验序号 | 双氧水体积 | 催化剂 | 待测数据 |
| a | 15mL | 无 | |
| b | 15mL | 0.5g CuO | |
| c | 15mL | 0.5g MnO2 |
②为探究CuO在实验b中是否起催化作用,除与
a比较外,还应补充以下实验(不必写具体操作):
A.证明CuO化学性质在反应前后是否改变;
B. .
Ⅱ.摩尔盐[(NH4)2SO4?FeSO4?6H2O]

在空气中比一般亚铁盐稳定,是化学分析中常用的还原剂.某研究性学习小组用图2所示的实验装置来制取摩尔盐,实验步骤如下,回答下列问题:
(1)用30%的NaOH溶液和废铁屑(含少量油污、铁锈、FeS等)混合、煮沸、冷却、分离,将分离出的NaOH溶液装入③中.
(2)利用容器②的反应,向容器①中通入氢气,应关闭活塞 ,打开活塞 (填字母).向容器①中通入氢气的目的是 .
(3)待锥形瓶中的铁屑快反应完时,关闭活塞B、C,打开活塞A,继续产生的氢气会将锥形瓶中的硫酸亚铁(含极少部分未反应的稀硫酸)压到饱和硫酸铵溶液的底部.在常温下放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵,抽滤,制得硫酸亚铁铵晶体.图3是抽滤装置的一部分,其中正确的是 .(填A或B)
(4)为了确定产品中亚铁离子的含量,研究小组用滴定法来测定.若取产品24.50g配成100mL溶液,取出10.00mL用0.1000mol?L-1KMnO4酸性溶液滴定,消耗KMnO4溶液10.00mL.
已知高锰酸钾与Fe2+的离子方程式为:MnO
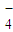 +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O试求产品中摩尔盐的质量分数 .(NH4)2SO4?FeSO4?6H2O的相对分子质量为392.