题目内容
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置. 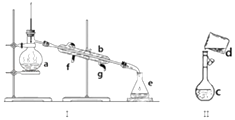
(1)写出下列仪器的名称:a.b.c. .
(2)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是 , 将仪器补充完整后进行实验,温度计水银球的位置在处.冷凝水由(填f或g)口通入.
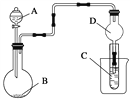
(3)现需配制0.1mol/L CuSO4溶液450mL,装置II是某同学转移溶液的示意图.
①图中的错误是 . 除图中给出的仪器和分析天平外,为完成实验还需的仪器有: .
②根据计算得知,需称取的胆矾的质量为g.
③在100mL某浓度的CuSO4溶液中加入一质量为45.0g的铁棒,反应一段时间后,取出洗净,干燥后称量,称得质量变为46.6g.若反应后溶液的体积不变,所得溶液中FeSO4的物质的量浓度为mol/L.
【答案】
(1)蒸馏烧瓶;冷凝器(直形冷凝管);容量瓶
(2)酒精灯;蒸馏烧瓶支管口;g
(3)没有用玻璃棒引流;玻璃棒和胶头滴管;12.5;2
【解析】解:(1)由图可知仪器的名称为a.蒸馏烧瓶、b.冷凝器(直形冷凝管)、c.容量瓶,所以答案是:蒸馏烧瓶;冷凝器(直形冷凝管);容量瓶;(2)分离四氯化碳和酒精的混合物,选择蒸馏装置,需要酒精灯加热,则图中缺少仪器为酒精灯,温度计水银球的位置在蒸馏烧瓶支管口处.冷凝水由g口通入,所以答案是:酒精灯;蒸馏烧瓶支管口;g;(3)①图中的错误是没有用玻璃棒引流;除图中给出的仪器和分析天平外,为完成实验还需的仪器有玻璃棒和胶头滴管,
所以答案是:没有用玻璃棒引流;玻璃棒和胶头滴管;
②选择500mL容量瓶,需称取的胆矾的质量为0.5L×0.1mol/L×250g/mol=12.5 g,所以答案是:12.5;
③
Fe+ | CuSO4=FeSO4+ | Cu | △m |
1 | 8 | ||
n | (46.6g﹣45.0g) |
n=0.2mol,反应后溶液的体积不变,仍为0.1L,则所得溶液中FeSO4的物质的量浓度为 ![]() =2 mol/L,
=2 mol/L,
所以答案是:2.
【考点精析】本题主要考查了配制一定物质的量浓度的溶液的相关知识点,需要掌握配制物质的量浓度溶液时,先用烧杯加蒸馏水至容量瓶刻度线1cm~2cm后,再改用交投滴管加水至刻度线才能正确解答此题.

 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案【题目】下表是周期表中的一部分,根据①﹣⑩在周期表中的位置,用元素符号或化学式回答下列问题:
族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | |||||||
2 | ④ | ⑦ | ⑧ | ⑩ | ||||
3 | ② | ③ | ⑤ | ⑥ | ⑨ |
(1)表中元素,化学性质最不活泼的是 , 只有负价而无正价的是 , 还原性最强的单质是 , 可用于制半导体材料的元素是;
(2)最高价氧化物的水化物酸性最强的是 , 呈两性的是 , 最高价氧化物的水化物碱性最强的是 , 电子式为;
(3)在②、③、④、⑤、⑥、⑦、⑧、⑨中,原子半径最大的是;
(4)比较⑥⑦⑨氢化物的稳定性最弱的是;
(5)③元素单质和②元素最高价氧化物对应的水化物相互反应的离子方程式为;
(6)铍(Be)位于元素周期表中第二周期第ⅡA族.相同条件下,单质铍与酸反应比单质锂与酸反应更加(填“剧烈”或“缓慢”),写出铍与盐酸反应的化学方程式 .