题目内容
8.化学与社会、生活密切相关.下列有关说法错误的是( )| A. | 明矾中铝离子水解产生的胶体具有很强的吸附作用而常用于净水 | |
| B. | 地球上99%以上的溴蕴藏在大海中,因此溴被称为“海洋元素” | |
| C. | 目前加碘盐中添加的含碘物质是KI,可用氯水和淀粉溶液鉴定食盐是否加碘 | |
| D. | 为减少污染、提高燃烧效率,可将煤气化或液化获得清洁燃料 |
分析 A.明矾溶解后溶液中铝离子水解生成氢氧化铝胶体具有吸附性;
B.地球上99%以上的溴都蕴藏在汪洋大海中;
C.加碘盐中添加的含碘物质是KIO3;
D.将煤气化或液化可以除去硫,减少对环境的污染.
解答 解:A.明矾溶解后溶液中铝离子水解生成氢氧化铝胶体具有吸附性,吸附悬浮在水中的杂质起到净水作用,故A正确;
B.地球上99%以上的溴都蕴藏在汪洋大海中,故溴有“海洋元素”的美称,故B正确;
C.加碘盐中添加的含碘物质不是KI是KIO3,用食醋、水和淀粉KI试纸检验加碘食盐中是否加碘,酸性溶液中IO3-、I-反应生成I2,与淀粉溶液作用显蓝色,故C错误;
D.将煤气化或者液化,可以除去硫元素,减少对环境的污染,故D正确;
故选C.
点评 本题考查了化学与生活中的化学知识分析判断,主要是物质性质的理解应用,掌握基础是关键,题目难度不大.

练习册系列答案
相关题目
16.下列有关摩尔的叙述正确的是( )
| A. | 表示物质数量的单位 | |
| B. | 用巨大数量的微粒集体表示物质的量的单位 | |
| C. | 表示物质的质量单位 | |
| D. | 既表示物质的质量又表示物质微粒的数量单位 |
3.设NA为阿伏加德罗常数,下列叙述正确的是( )
| A. | 1molCl2参加化学反应获得的电子数都是2NA | |
| B. | 6.4 gO2与O3的混合物中所含O原子数一定为0.4NA | |
| C. | 含4nmol HCl的浓盐酸与足量的MnO2加热反应,生成的Cl2分子数为nNA | |
| D. | 1mol某气体的体积为22.4L,该气体的状况一定是标准状况 |
13.下列变化过程不涉及氧化还原反应的是( )
| A. | 将一小块钠放在石棉网上加热,生成淡黄色物质 | |
| B. | 向新制氯水中加入足量亚硫酸钠溶液,氯水褪色 | |
| C. | 向纯碱溶液中滴加酚酞,溶液变红色 | |
| D. | 向氢碘酸中滴加FeCl3溶液,产生棕色物质 |
20.某有机原料的结构简式如图,下列有关该有机物的叙述正确的是( )
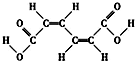

| A. | 该物质有三种3种不同化学环境的氢(不考虑顺反异构) | |
| B. | 1mol该有机物可以和2mol NaOH反应,但不能用Na2CO3溶液区分该有机物和CH3COOCH2CH3 | |
| C. | 该有机物能发生加成反应不能发生取代反应 | |
| D. | 该有机物与乙酸互为同系物 |
17.硫酸钠和氯化钠溶液等体积混合后,钠离子浓度为0.7mol•L-1,硫酸根离子的浓度为0.2mol•L-1,则混合液中氯离子的浓度为( )
| A. | 0.15mol•L-1 | B. | 0.3mol•L-1 | C. | 0.45mol•L-1 | D. | 0.2mol•L-1 |
18.在某恒温恒容密闭容器中,发生反应:A(g)+B(g)?2C(g)△H=-Q kJ/mol(Q>0),保持其它条件不变,只改变起始添加量,测得相关数据如表所示
下列说法中错误的是( )
| 起始加入量(mol) | 平衡时 | ||||
| A | B | C | A或C转化率(%) | C的物质的量分数(%) | 放出或吸收热量(kJ) |
| 1 | 1 | 0 | α1 | φ1 | Q1 |
| 0 | 0 | 2 | α2 | φ2 | Q2 |
| 2 | 2 | 0 | α3 | φ3 | Q3 |
| A. | α1+α2=1; φ2=φ1 | B. | α1=α3;Q1+Q2=Q | ||
| C. | φ3=φ1=φ2; Q3=2Q1 | D. | φ3=2φ1; Q3=Q1 |