题目内容
12.下列说法中正确的是( )| A. | 由Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑可知,酸性H2SiO3>H2CO3 | |
| B. | 氢氟酸需要密封存放在橡胶塞的玻璃试剂瓶中 | |
| C. | 向硅酸钠溶液中加入盐酸产生白色沉淀,过量时沉淀溶解 | |
| D. | 瓷坩埚、氧化铝坩埚均不可作为融化NaOH固体的装置 |
分析 A.硅酸的酸性比碳酸弱;
B.氢氟酸能与玻璃中的二氧化硅反应;
C.强酸能制弱酸,硅酸钠与盐酸反应生成硅酸,硅酸不溶于水,和盐酸也不反应;
D.二氧化硅、氧化铝能和氢氧化钠反应生成偏铝酸钠.
解答 解:A.硅酸的酸性比碳酸弱,反应Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑,是利用的难挥发性酸酐制备易挥发性酸酐,故A错误;
B.氢氟酸能与玻璃中的二氧化硅反应,应保存在塑料瓶中,故B错误;
C.盐酸的酸性比硅酸的强,因此硅酸钠溶液与稀盐酸溶液能发生反应,方程式为:Na2SiO3+2HCl═2NaCl+H2SiO3↓,生成的硅酸不溶于水,并与盐酸也不反应,过量时沉淀不溶解,故C错误;
D.二氧化硅、氧化铝能和氢氧化钠反应生成偏铝酸钠,所以瓷坩埚、氧化铝坩埚均不可作为融化NaOH固体的装置,故D正确;
故选:D.
点评 本题主要考查了物质的性质与运用,难度不大,注意制备原理的掌握.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
7.NA表示阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 1mol苯乙烯中含有的碳碳双键数为4NA | |
| B. | 7.8g过氧化钠晶体中含有0.1NA个O${\;}_{2}^{2-}$ | |
| C. | 标准状况下,22.4LNO2中含有NA个NO2分子 | |
| D. | 1mol•L-1NH4Cl溶液中,NH${\;}_{4}^{+}$的数目小于NA |
17.下列实验装置不能达到实验目的是( )
| A. | 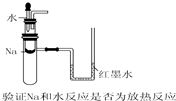 | B. |  | ||
| C. |  | D. | 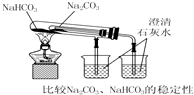 |
1.已知铍(Be)的原子序数为4,下列对铍及其化合物的叙述中正确的是( )
| A. | Be(OH)2可能具有两性 | |
| B. | 氯化铍中铍原子的最外层电子数是8个 | |
| C. | 氢氧化铍的碱性比氢氧化钙强 | |
| D. | 单质铍可和冷水剧烈反应产生氢气 |
2.下列关于有机物的说法正确的是( )
| A. | 实验室制备硝基苯加入试剂的顺序为:先加入浓硫酸,再滴加苯,最后滴加浓硝酸 | |
| B. | 蔗糖和葡萄糖不是同分异构体,但属同系物 | |
| C. | 可用金属钠区分乙酸、乙醇和苯 | |
| D. | 石油裂解和煤的干馏都是化学变化,而石油的分馏和煤的气化都是物理变化 |
 在实验室里制取乙烯的反应为:
在实验室里制取乙烯的反应为: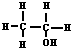 $→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O
$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O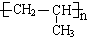 .
.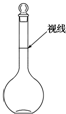 实验室配制500mL 0.2mol•L-1的Na2SO4溶液,实验操作步骤有:
实验室配制500mL 0.2mol•L-1的Na2SO4溶液,实验操作步骤有: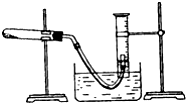 某学生利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量.实验步骤如下:
某学生利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量.实验步骤如下: