题目内容
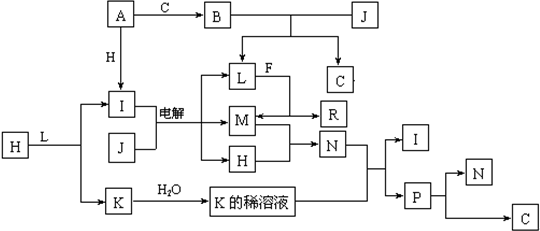
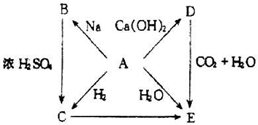
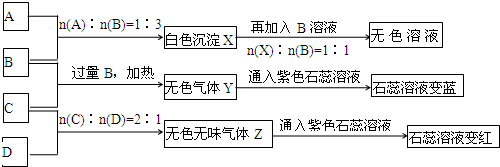
A、B、C、D、E、F、G为常见物质,其中C为淡黄色固体.甲、乙、丙为常见气体.各物质的转化关系如图所示.

回答下列问题:
(1)C的名称是______;D的俗称______;F的化学式______;
A+甲→C的反应条件是______.
(2)在一定条件下,甲+乙→F,该反应属于______.
①氧化还原反应②非氧化还原反应③化合反应④分解反应 ⑤复分解反应⑥置换反应⑦离子反应
(3)写出下列变化的离子方程式.
①A+F→E+乙:______.
②D+F+丙→G:______.

回答下列问题:
(1)C的名称是______;D的俗称______;F的化学式______;
A+甲→C的反应条件是______.
(2)在一定条件下,甲+乙→F,该反应属于______.
①氧化还原反应②非氧化还原反应③化合反应④分解反应 ⑤复分解反应⑥置换反应⑦离子反应
(3)写出下列变化的离子方程式.
①A+F→E+乙:______.
②D+F+丙→G:______.
A、B、C、D、E、F、G为常见物质,其中C为淡黄色固体,且C是化合物,甲是气体,所以C是过氧化钠,甲是氧气,A和氧气反应生成B,B和氧气反应生成过氧化钠,则A是钠,B是氧化钠,钠和F反应生成气体乙,且乙是常见气体,则乙是氢气,E能和气体丙反应生成G,C和丙反应生成氧气和D,丙是气体,D能和丙、F反应生成G,则丙是二氧化碳,D是碳酸钠,F是水,E是氢氧化钠,G是碳酸氢钠.
(1)通过以上分析知,C是过氧化钠,其名称是过氧化钠,D是碳酸钠,其俗称是纯碱或苏打,F是水,其化学式为:H2O,钠在氧气中燃烧生成过氧化钠,所以其条件是点燃,
故答案为:过氧化钠;纯碱或苏打;H2O;点燃;
(2)在一定条件下,氢气和氧气反应生成水,该反应中有元素化合价变化,所以是氧化还原反应,且该反应是化合反应,故选①③
(3)①钠和水反应生成氢氧化钠和氢气,离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,
故答案为2Na+2H2O═2Na++2OH-+H2↑;
②碳酸钠和水、二氧化碳反应生成碳酸氢钠,离子反应方程式为:CO32-+H2O+CO2═2HCO3-,
故答案为:CO32-+H2O+CO2═2HCO3-.
(1)通过以上分析知,C是过氧化钠,其名称是过氧化钠,D是碳酸钠,其俗称是纯碱或苏打,F是水,其化学式为:H2O,钠在氧气中燃烧生成过氧化钠,所以其条件是点燃,
故答案为:过氧化钠;纯碱或苏打;H2O;点燃;
(2)在一定条件下,氢气和氧气反应生成水,该反应中有元素化合价变化,所以是氧化还原反应,且该反应是化合反应,故选①③
(3)①钠和水反应生成氢氧化钠和氢气,离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,
故答案为2Na+2H2O═2Na++2OH-+H2↑;
②碳酸钠和水、二氧化碳反应生成碳酸氢钠,离子反应方程式为:CO32-+H2O+CO2═2HCO3-,
故答案为:CO32-+H2O+CO2═2HCO3-.

练习册系列答案
相关题目