题目内容
塑化剂是一种对人体有害的物质.增塑剂DCHP可由邻苯二甲酸酐与环己醇反应制得:下列说法正确的是( )


| A、环己醇分子中所有的原子可能共平面 |
| B、1mol DCHP可与含4mol NaOH的溶液完全反应 |
| C、DCHP能发生加成、取代反应,不能发生消去反应 |
| D、DCHP易溶于水 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:A.环己醇中含5个亚甲基,均为四面体结构;
B.-COOC-与NaOH反应;
C.DCHP中含苯环和-COOC-,不存在能发生消去反应的官能团;
D.DCHP属于酯类物质.
B.-COOC-与NaOH反应;
C.DCHP中含苯环和-COOC-,不存在能发生消去反应的官能团;
D.DCHP属于酯类物质.
解答:
解:A.环己醇中含5个亚甲基,均为四面体结构,则不可能所有原子共面,故A错误;
B.-COOC-与NaOH反应,则1mol DCHP可与2mol NaOH完全反应,故B错误;
C.DCHP中含苯环和-COOC-,则苯环发生加成反应,-COOC-可发生取代反应,不能发生消去反应,故C正确;
D.DCHP属于酯类物质,不溶于水,故D错误;
故选C.
B.-COOC-与NaOH反应,则1mol DCHP可与2mol NaOH完全反应,故B错误;
C.DCHP中含苯环和-COOC-,则苯环发生加成反应,-COOC-可发生取代反应,不能发生消去反应,故C正确;
D.DCHP属于酯类物质,不溶于水,故D错误;
故选C.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重苯、酯性质的考查,选项A为易错点,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
美国科学家成功开发便携式固体氧化物燃料电池,它以丙烷气体为燃料,每填充一次燃料,大约可连续24小时输出50W的电力.一极通人空气,另一极通人丙烷气体,电解质是固态氧化物,在熔融状态下能传导O2-,下列对该燃料电池的说法不正确的是( )
| A、在熔融电解质中,O2-由正极移向负极 |
| B、以该电池为电源实现铁上镀银,通入空气的一极与银电极相连 |
| C、通丙烷的电极为电池负极,发生的电极反应为:C3H8-20e-+10O2-=3CO2+4H2O |
| D、电路中每流过5mol电子,必有5.6L丙烷被完全氧化 |
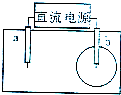 取一张紫色石蕊试纸,用饱和NaCl溶液浸湿;如图,用两根铅笔芯作电极,接通直流电源,一段时间后,发现b电极与试纸接触处出现一个白色的圆,圆的边缘呈浅红色.则下列说法错误的是( )
取一张紫色石蕊试纸,用饱和NaCl溶液浸湿;如图,用两根铅笔芯作电极,接通直流电源,一段时间后,发现b电极与试纸接触处出现一个白色的圆,圆的边缘呈浅红色.则下列说法错误的是( )| A、a电极与电源的负极相连 |
| B、b电极生成氧气 |
| C、b电极附近存在Cl2+H2O═HCl+HClO |
| D、a电极附逅溶液的pH变大 |
关于铯(Cs)及其化合物的性质,说法正确的是( )
| A、金属铯的熔点比金属钠高 |
| B、NaOH比CsOH的碱性强 |
| C、Cs与H2O能剧烈反应,甚至发生爆炸 |
| D、碳酸铯难溶于水 |
氢化钠(NaH)是一种重要的无机化合物,它与水作用可产生H2,下列说法正确的是( )
| A、该化合物为共价化合物 |
| B、4.8g NaH含有的离子个数为1.204×1022 |
| C、Na+的氧化性大于>H+ |
| D、NaH与水反应是氧化还原反应 |
将5.1g镁和铝投入500mL 2mol/L的盐酸中,生成氢气0.5g,金属完全溶解;再加入4mol/L的NaOH溶液,生成沉淀的质量最多是( )
| A、22.1g | B、8.5g |
| C、10.2g | D、13.6g |
在一定条件下,将2molX和3molY 充入一密闭容器中,发生如下可逆反应:nX(g)+3Y(g)?2Z(g) 达到平衡时,X的转化率为a%,Y的转化率为b%,若a<b,则n的值为( )
| A、1 | B、2 | C、3 | D、4 |
下列叙述的有关性质,可能属于金属晶体的是( )
| A | 由分子间作用力结合而成,熔点低 |
| B | 固体或熔融状态易导电,熔点在1000℃左右 |
| C | 由共价键结合成网状结构,熔点高 |
| D | 固体不导电,但溶于水或熔融后能导电 |
| A、A | B、B | C、C | D、D |
导致下列现象的主要原因与排放氮的氧化物无关的是( )
| A、酸雨 | B、臭氧层空洞 |
| C、温室效应 | D、光化学烟雾 |