题目内容
下列叙述的有关性质,可能属于金属晶体的是( )
| A | 由分子间作用力结合而成,熔点低 |
| B | 固体或熔融状态易导电,熔点在1000℃左右 |
| C | 由共价键结合成网状结构,熔点高 |
| D | 固体不导电,但溶于水或熔融后能导电 |
| A、A | B、B | C、C | D、D |
考点:金属晶体
专题:化学键与晶体结构
分析:A.由分子间作用力结合而成属于分子晶体,影响熔沸点的因素是分子间作用力的大小;
B.固体或熔融状态易导电,可能为金属晶体;
C.由共价键结合成网状结构,熔点高为原子晶体;
D.固体不导电,但溶于水或熔融后能导电属于离子晶体.
B.固体或熔融状态易导电,可能为金属晶体;
C.由共价键结合成网状结构,熔点高为原子晶体;
D.固体不导电,但溶于水或熔融后能导电属于离子晶体.
解答:
解:A.由分子间作用力结合而成属于分子晶体,物质的相对分子质量越大,分子间作用力越强,沸点越高,反之,越弱越低,故A错误;
B.金属晶体中有电子,能导电,大多数在常温下为固体,熔点较高,所以固体或熔融状态易导电,熔点在1000℃左右可能属于金属晶体,故B正确;
C.相邻原子之间通过强烈的共价键结合而成的空间网状结构的晶体是原子晶体,该晶体以共价键形成的空间网状结构,无自由移动的带电微粒,不具备金属晶体的特征,属于原子晶体,故C错误;
D.含有自由移动的带电微粒(如离子、电子)的物质能导电,固体不导电,说明无自由移动的带电微粒,但溶于水或熔融后能导电可能为离子晶体,在熔融状态下能够电离出阴阳离子,所以熔融能够导电,故D错误;
故选B.
B.金属晶体中有电子,能导电,大多数在常温下为固体,熔点较高,所以固体或熔融状态易导电,熔点在1000℃左右可能属于金属晶体,故B正确;
C.相邻原子之间通过强烈的共价键结合而成的空间网状结构的晶体是原子晶体,该晶体以共价键形成的空间网状结构,无自由移动的带电微粒,不具备金属晶体的特征,属于原子晶体,故C错误;
D.含有自由移动的带电微粒(如离子、电子)的物质能导电,固体不导电,说明无自由移动的带电微粒,但溶于水或熔融后能导电可能为离子晶体,在熔融状态下能够电离出阴阳离子,所以熔融能够导电,故D错误;
故选B.
点评:本题考查了晶体判别,根据晶体的构成微粒、微粒间的作用力以及性质来分析解答,注意各晶体的性质特点,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质中属于非电解质,但放入水中后所得溶液导电性明显增强的是( )
| A、金属钠 | B、三氧化硫 |
| C、氯化钠 | D、乙醇 |
塑化剂是一种对人体有害的物质.增塑剂DCHP可由邻苯二甲酸酐与环己醇反应制得:下列说法正确的是( )


| A、环己醇分子中所有的原子可能共平面 |
| B、1mol DCHP可与含4mol NaOH的溶液完全反应 |
| C、DCHP能发生加成、取代反应,不能发生消去反应 |
| D、DCHP易溶于水 |
下列各项叙述中,正确的是( )
| A、C6H5CH2CH2OH与C6H5OH互为同系物 |
| B、H2O与D2O互为同素异形体 |
C、 与 与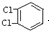 互为同分异构体 互为同分异构体 |
| D、等物质的量的乙醇和乙烯完全燃烧时所需氧气的质量相等 |
下列过程能生成离子键的是( )
| A、白磷在空气中燃烧 |
| B、镁在空气中逐渐失去金属光泽 |
| C、硫磺在空气中点燃 |
| D、氢碘酸与氯气反应 |
下列关于离子键的说法中,正确的是( )
| A、阴阳离子间相互吸引即离子键 |
| B、非金属元素所组成的化合物中不可能有离子键 |
| C、一个阳离子只可与一个阴离子之间存在离子键 |
| D、活泼金属与非金属化合时一般形成离子键 |
从分类角度看,下列说法正确的是( )
| A、雾属于分散系中的胶体 |
| B、氨气属于非电解质,Cu属于电解质 |
| C、Na2CO3溶液显碱性,说明Na2CO3属于碱 |
| D、二氧化氮和二氧化硫都是酸性氧化物 |
下列实验现象与氧化还原反应有关的是( )
| A、铁和铝在浓硫酸和浓硝酸中发生钝化 |
| B、向硅酸钠溶液中滴加适量的稀盐酸,有透明的凝胶形成 |
| C、NO2通入水中,气体由红棕色逐渐转变为无色 |
| D、硫酸铁溶液中滴加硫氰化钾溶液变红 |