题目内容
实验室常用浓盐酸和二氧化锰反应来制取少量氯气,反应的化学方程式为:
MnO2 + 4HCl(浓) MnCl2 + Cl2↑ + 2H2O。
MnCl2 + Cl2↑ + 2H2O。
取8.7g的MnO2与50mL足量的浓盐酸发生反应制取氯气。求:
(1)生成的还原产物的物质的量是多少?
(2)(忽略Cl2的溶解)产生的氯气在标准状况下的体积为多少?
(3)反应中被氧化的HCl的物质的量是多少?
MnO2 + 4HCl(浓)
 MnCl2 + Cl2↑ + 2H2O。
MnCl2 + Cl2↑ + 2H2O。取8.7g的MnO2与50mL足量的浓盐酸发生反应制取氯气。求:
(1)生成的还原产物的物质的量是多少?
(2)(忽略Cl2的溶解)产生的氯气在标准状况下的体积为多少?
(3)反应中被氧化的HCl的物质的量是多少?
(1)0.1mol (2 ) 2.24L ( 3 ) 0.2mol
试题分析:(1)二氧化锰的摩尔质量是87g/mol
则根据 n=
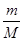 可知,8.7二氧化锰的物质的量=8.7g÷87g/mol=0.1mol
可知,8.7二氧化锰的物质的量=8.7g÷87g/mol=0.1mol根据方程式可知,二氧化锰是氧化剂,其还原产物是MnCl2
则根据原子守恒可知,还原产物氯化锰的物质的量是0.1mol
(2)根据方程式可知
MnO2 + 4HCl(浓)
 MnCl2 + Cl2↑ + 2H2O
MnCl2 + Cl2↑ + 2H2O1mol 1mol
0.1mol 0.1mol
即生成的氯气是0.1mol
标准状况下气体的摩尔体积是22.4L/mol
则根据n=
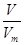 可知,生成的氯气在标准状况下的体积V=0.1mol×22.4L/mol=2.24L
可知,生成的氯气在标准状况下的体积V=0.1mol×22.4L/mol=2.24L(3)氯气是氧化产物,则根据氯原子守恒可知反应中被氧化的HCl的物质的量是0.1mol×2=0.2mol

练习册系列答案
相关题目
 Cl2↑+MnCl2+2H2O
Cl2↑+MnCl2+2H2O SiC+2CO↑反应中,氧化剂和还原剂的质量比为
SiC+2CO↑反应中,氧化剂和还原剂的质量比为 与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色。据此判断下列说法正确的是
与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色。据此判断下列说法正确的是