题目内容
下列有关物质性质的应用正确的是( )
| A、生石灰能与水反应,可用来干燥氯气 |
| B、二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 |
| C、液氨气化时要吸收大量的热,可用作制冷剂 |
| D、氯化铝是一种电解质,可用于电解法制铝 |
考点:硅和二氧化硅,氨的化学性质,镁、铝的重要化合物
专题:元素及其化合物
分析:A.氯气可与碱性物质反应;
B.二氧化硅可与氢氟酸反应;
C.根据制冷剂的原理判断;
D.氯化铝不导电.
B.二氧化硅可与氢氟酸反应;
C.根据制冷剂的原理判断;
D.氯化铝不导电.
解答:
解:A.氯气可与氢氧化钙反应,不能用碱性干燥剂干燥,故A错误;
B.二氧化硅可与氢氟酸反应生成四氟化硅,故B错误;
C.液氨沸点较高,气化时要吸收大量的热,可用作制冷剂,故C正确;
D.氯化铝为共价化合物,熔融状态下不导电,故D错误.
故选C.
B.二氧化硅可与氢氟酸反应生成四氟化硅,故B错误;
C.液氨沸点较高,气化时要吸收大量的热,可用作制冷剂,故C正确;
D.氯化铝为共价化合物,熔融状态下不导电,故D错误.
故选C.
点评:本题综合考查元素化合物知识,为高考常见题型,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
下列说法不正确的是( )
| A、体系有序性越高,熵值就越低 |
| B、一杯热水变冷是焓减少的过程 |
| C、吸热反应不可以自发进行 |
| D、同种物质气态时熵值最大 |
下列物质分类正确的是( )
| A、SO2、SiO2、CO均为酸性氧化物 |
| B、稀豆浆、硅酸、氯化铁溶液均为胶体 |
| C、福尔马林、水玻璃、氨水均为混合物 |
| D、烧碱、冰醋酸、四氯化碳均为电解质 |
某温度时,在体积为1L的密闭容器中,X、Y、Z三种气体浓度的变化如图I所示,若其它条件不变,当温度分别为Tl和T2时,Y的体积百分含量与时间关系如图II所示. 则下列结论正确的是( )


| A、该反应的热化学方程式为:X(g )+3Y(g)?2Z(g);△H>0 |
| B、达到平衡后,若其他条件不变,通入稀有气体,平衡向正反应方向移动 |
| C、达到平衡后,若其他条件不变,减小体积,平衡向正反应方向移动 |
| D、若其它条件不变,升高温度,正、逆反应速率均增大,X的转化率增大 |
2008年,美籍华裔科学家钱永健获得2008年度诺贝尔化学奖.16岁时,他凭借一个金属易受硫氰酸盐腐蚀的调查项目,荣获“美国西屋天才奖”.下列叙述正确的是 ( )
| A、金属腐蚀就是金属失去电子被还原的过程 |
| B、将水库中的水闸(钢板)与外加直流电源的负极相连,正极连接到一块废铁上可防止水闸被腐蚀 |
| C、纯银质物品久置表面变暗,是银发生吸氧腐蚀的结果 |
| D、钢板上的铁铆钉处在潮湿的空气中直接发生反应:Fe-3e-═Fe3+,继而形成铁锈 |
50℃时,下列各溶液中,离子的物质的量浓度关系正确的是( )
| A、pH=4的醋酸中:c(H+)=4.0mol?L-1 | ||
B、饱和小苏打溶液中:c(Na+)=c(HCO
| ||
| C、pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol?L-1 | ||
| D、0.1mol/L NaOH溶液和0.2mol/L CH3COOH溶液等体积混合:c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) |
下列物质中,含有自由氯离子的是( )
①食盐溶液 ②氯化氢溶液 ③氯酸钾 ④液态氯化氢 ⑤氯水.
①食盐溶液 ②氯化氢溶液 ③氯酸钾 ④液态氯化氢 ⑤氯水.
| A、①②③ | B、②③④ |
| C、③④⑤ | D、①②⑤ |
下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是( )
| A、1,3-丁二烯(CH2=CH-CH=CH2)与等物质的量的Br2发生加成反应 |
B、2-氯丁烷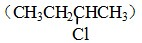 与NaOH乙醇溶液共热发生消去HCl分子的反应 与NaOH乙醇溶液共热发生消去HCl分子的反应 |
| C、丙炔与足量的溴水发生的加成反应 |
| D、CH2=CH-CH3与HBr发生的加成反应 |