题目内容
19.已知标准状况下,m1g气体G1与m2g气体G2的分子数相同,则:(1)同温同压下G1与G2的密度比为m1:m2(用m1、m2表示);
(2)同温同质量的G1和G2的分子数比为m2:m1(用m1、m2表示);
(3)同温同压下同体积G1和G2的质量比为m1:m2(用m1、m2表示);
(4)两密闭容器,若温度、密度相同(m1>m2),则其压强(p)G1<G2(填>、=、<).
分析 标准状况下,m1g气体G1与m2g气体G2的分子数相同,所以物质的量是相等的,根据公式m=ρV,m=nM=$\frac{N}{{N}_{A}}$M进行计算即可.
解答 解:标准状况下,m1g气体G1与m2g气体G2的分子数相同,所以物质的量是相等的,根据公式m=nM,所以摩尔质量之比等于质量之比,即为m1:m2,
(1)根据公式M=ρVm,同温同压下,气体的Vm是相等的,所以G1与G2的密度比为等于摩尔质量之比,即为m1:m2,故答案为:m1:m2;
(2)根据公式m=$\frac{N}{{N}_{A}}$M,同温同质量的G1和G2的分子数之比等于摩尔质量的倒数之比,即为m2:m1;故答案为:m2:m1;
(3)同温同压下,二者的Vm是相等的.同体积G1和G2的物质的量是相等的,所以质量比为摩尔质量之比,即为m1:m2,故答案为:m1:m2;
(4)两密闭容器,若温度、密度相同(m1>m2),根据公式PV=nRT=$\frac{ρV}{M}$RT,则其压强(p)和摩尔质量的乘积是一个常数,M越大,所以压强越小,二者摩尔质量之比等于质量之比,即为m1:m2,m1>m2,所以压强:G1<G2,故答案为:<.
点评 本题考查学生物质的量的有关公式的应用以及阿伏伽德罗定律的应用知识,注意知识的迁移应用是关键,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.偏二甲肼(C2H8N2)是一种高能燃料,燃烧产生巨大能量,可作为航天运载火箭的推动力.下列叙述正确的是( )
| A. | 6.02×1023个偏二甲肼分子的质量是60g | |
| B. | 偏二甲肼的摩尔质量是60g | |
| C. | 标况下,1mol偏二甲肼的体积为22.4L | |
| D. | 6g偏二甲肼中电子数目为6NA(NA表示阿伏伽德罗常数) |
14.对于HD的描述,不正确的是( )
| A. | 是一种非金属单质 | |
| B. | HD能在氯气中燃烧生成HCl和DCl气体 | |
| C. | 是一种化合物 | |
| D. | 在受热条件下,HD能还原氧化铜 |
4.下列各组离子在指定的溶液中能大量共存的是( )
| A. | 无色溶液中:K+、Cu2+、Na+、SO42- | |
| B. | 加入Al能放出H2的溶液中:Cl-、HCO3-、NO3-、NH4+ | |
| C. | 强酸性溶液中:Fe2+、Al3+、NO3-、Cl- | |
| D. | 酚酞试液显红色的溶液中:Ba2+、Na+、AlO2- |
11.下列说法正确的是( )
| A. | 纤维素从化学成分看,它是一种多糖.食物中的纤维素不仅能为人体提供能量,也能促进肠道蠕动、吸附排出有害物质 | |
| B. | 某物质的结构为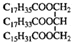 ,与其互为同分异构体,且完全水解后产物相同的油脂有3种 ,与其互为同分异构体,且完全水解后产物相同的油脂有3种 | |
| C. | 蛋白质的检验方法有许多种,而与双缩脲试剂作用而产生紫玫瑰色的颜色反应是最常见的方法之一 | |
| D. | 糖类、油脂、蛋白质是人类最主要的能量来源,它们都是天然高分子化合物 |
8.人体血红蛋白中含有Fe2+,如果大量食用烤肠(含亚硝酸盐)会使人中毒,因为亚硝酸盐会使Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与O2的结合能力,服用维生素C可以缓解亚硝酸盐的中毒,这说明维生素C具有( )
| A. | 酸性 | B. | 碱性 | C. | 氧化性 | D. | 还原性 |
13.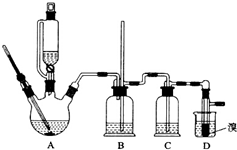 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:
CH3CH2OH $→_{170℃}^{H_{2}SO_{4}(浓)}$ CH2=CH2
CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.
用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
有关数据列表如下:
回答下列问题:
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是d;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入c,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制各反应已经结束的最简单方法是溴的颜色完全褪去;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”“下”);
(5)若产物中有少量未反应的Br2,最好用b洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用蒸馏的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.
 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH $→_{170℃}^{H_{2}SO_{4}(浓)}$ CH2=CH2
CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.
用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是d;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入c,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制各反应已经结束的最简单方法是溴的颜色完全褪去;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”“下”);
(5)若产物中有少量未反应的Br2,最好用b洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用蒸馏的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.