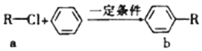
题目内容
【题目】下列指定反应的离子方程式正确的是( )
A. 饱和Na2CO3溶液与BaSO4固体反应:CO32-+Ba2+![]() BaCO3
BaCO3
B. NH4HCO3溶液和过量Ca(OH)2溶液混合:Ca2++NH4++HCO3-+2OH-===CaCO3↓+H2O+ NH3·H2O
C. NaClO与HI溶液反应:2ClO-+2H2O+2I-===I2+Cl2↑+4OH-
D. 电解氯化镁溶液:2Cl-+Mg2+![]() Cl2↑+Mg
Cl2↑+Mg
【答案】B
【解析】
按照离子方程式的书写步骤:写、拆、删、查,分析判断正误。
A项:BaSO4难溶于水,不能拆写。饱和Na2CO3溶液使BaSO4转化的离子方程式为:CO32-+BaSO4![]() BaCO3+SO42- ,A项错误;
BaCO3+SO42- ,A项错误;
B项:Ca(OH)2溶液过量,NH4+、HCO3-完全反应,B项正确;
C项:NaClO作氧化剂,被还原成Cl-而不是Cl2,酸性溶液中也不会生成OH-,离子方程式应写ClO-+2I-+2H+=I2+Cl-+H2O,C项错误;
D项:电解氯化镁溶液时,阴极氢离子得电子生成氢气,离子方程式应为:Mg2++2Cl-+2H2O![]() Cl2↑+H2↑+Mg(OH)2↓。
Cl2↑+H2↑+Mg(OH)2↓。
本题选B。

【题目】(I)工业上过氧化氢是重要的氧化剂和还原剂。常用于消毒、杀菌、漂白等。某化学兴趣小组的同学围绕过氧化氢开展了调查研究与实验,请你参与其中一起完成下列学习任务:
(1)该兴趣小组的同学查阅资料后发现H2O2为二元弱酸,其酸性比碳酸弱。请写出H2O2在水溶液中的电离方程式:____________________________。
(2)同学们用0.1000mol/L-1的酸性高锰酸钾标准溶液滴定某试样中过氧化氢的含量,反应原理为2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑。
①在该反应中,H2O2被_________(填“氧化”或“还原”)。
②滴定到达终点的现象是____________________________。
③用移液管吸取25.00mL试样置于锥形瓶中,重复滴定四次,每次消耗的酸性KMnO4标准溶液体积如下表所示:
第一次 | 第二次 | 第三次 | 第四次 | |
体积(mL) | 17.10 | 18.10 | 17.00 | 16.90 |
则试样中过氧化氢的浓度为__________mol/L-1。
(II)医学上常用酸性高锰酸钾溶液和草酸溶液的反应来测定血钙的含量。测定含量如下:取2mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀疏酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
(1)滴定时,用_____(填酸或碱)式滴定管装KMnO4溶液。
(2)下列操作会引起测定结果偏高的是______。
A.滴定管在盛装高锰酸钾前未润洗
B.滴定过程中,锥形瓶震荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.锥形瓶未用待测液润洗