题目内容
11.下列叙述中,可以肯定金属A比金属B的活动性强的是( )| A. | A原子最外层电子数比B原子最外层电子数少 | |
| B. | A的最高价氧化物对应水化物的碱性强于B的最高价氧化物对应水化物的碱性 | |
| C. | 1molA与足量酸反应生成的H2比1molB与足量酸反应生成的H2多 | |
| D. | 常温时,A、B均能导电,且导电性良好 |
分析 比较金属的活泼性可根据金属之间的置换反应及金属与酸反应置换氢气的难易程度判断,金属与水反应的难易程度,最高价氧化物的水化物碱性,原电池的正负极判断等方面判断,不能从电子层的多少、最外层电子数的多少以及生成氢气的多少的角度判断.
解答 解:A、如金属不位于同一主族,则不能根据电子层数的多少来判断金属的活泼性强弱,故A错误;
B、最高价氧化物的水化物碱性越强,其元素的非金属性越强,A的最高价氧化物对应水化物的碱性强于B的最高价氧化物对应水化物的碱性,可以说明金属A的活动性比金属B的活动性强,故B正确;
C、产生氢气的多少取决于金属失去电子数的多少,金属的活泼性与得失电子难易有关,与得失电子数目无关,故C错误;
D、金属的导电性属于物理性质,不能根据导电性来判断金属性的强弱,故D错误;
故选B.
点评 本题考查了金属活泼性的判断方法,要注意的是:金属的金属性强弱与得失电子的难易有关,与得失电子的多少无关,题目难度不大.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
1.当光束通过下列物质的时候,能观察到丁达尔效应的是( )
| A. | 豆浆 | B. | 硫酸铜溶液 | C. | 蒸馏水 | D. | 食盐水 |
2.从平时学生实验中我们发现,同学们在进行实验时出现许多不正确的操作方式,希望同学们在今后的实验中,应该克服不规范的操作.请找出下列图示中正确的实验操作( )
| A. |  除去CO2中的HCl | B. |  蒸发氯化钠溶液 | ||
| C. |  稀释浓硫酸 | D. |  过滤 |
6.下列说法中错误的是( )
| A. | 若XY4分子中X原子处于正四面体的中心,则XY4分子为非极性分子 | |
| B. | C2H5OH与C2H5Br相比,前者的相对分子质量远小于后者,而沸点却远高于后者,其原因是前者的分子间存在氢键 | |
| C. | CO2与SiO2晶体熔化时,所克服的微粒间相互作用相同 | |
| D. | 短周期元素离子aXm+和bYn-具有相同的电子层结构,则a>b |
1.二氯化二硫(S2Cl2)在工业上用于橡胶的硫化.为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:
①干燥的氯气在110℃~140℃与硫反应,即可得S2Cl2粗产品.
②有关物质的部分性质如下表
设计实验装置图如下:

(1)上图中尾气处理装置不够完善,请你提出改进意见:在G和H之间增加干燥装置.
利用改进后的正确装置进行实验,请回答下列问题:
(2)B中反应的离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;E中反应的化学方程式:2S+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$S2Cl2.
(3)仪器B的名称是圆底烧瓶,C中的试剂是饱和食盐水,所起的作用是除去氯气中的氯化氢气体,粗S2Cl2产品收集在装置G中(填字母).
(4)将纯净的S2Cl2溶于足量的NaOH溶液中,发生的反应化学方程式为2S2Cl2+6NaOH═4NaCl+Na2SO3+3H2O+3S↓,
(5)为进一步检验(4)反应后溶液中大量存在的阴离子,某兴趣小组设计了如下实验:
①在所得液体中加入CS2,振荡,淡黄色固体溶解,混合液分层,该操作为萃取;
②进行分液(填操作名称),取所得上层清液继续进行实验;
③检验溶液中的阴离子(限选的试剂有:酚酞溶液、Ba(NO3)2溶液、AgNO3溶液、盐酸、稀HNO3、KMnO4溶液)
①干燥的氯气在110℃~140℃与硫反应,即可得S2Cl2粗产品.
②有关物质的部分性质如下表
| 物质 | 熔点/℃ | 沸点/℃ | 化学性质 |
| S | 112.8 | 444.6 | 略 |
| S2Cl2 | -77 | 137 | 遇水生成HCl、SO2、S 3000C以上完全分解 |

(1)上图中尾气处理装置不够完善,请你提出改进意见:在G和H之间增加干燥装置.
利用改进后的正确装置进行实验,请回答下列问题:
(2)B中反应的离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;E中反应的化学方程式:2S+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$S2Cl2.
(3)仪器B的名称是圆底烧瓶,C中的试剂是饱和食盐水,所起的作用是除去氯气中的氯化氢气体,粗S2Cl2产品收集在装置G中(填字母).
(4)将纯净的S2Cl2溶于足量的NaOH溶液中,发生的反应化学方程式为2S2Cl2+6NaOH═4NaCl+Na2SO3+3H2O+3S↓,
(5)为进一步检验(4)反应后溶液中大量存在的阴离子,某兴趣小组设计了如下实验:
①在所得液体中加入CS2,振荡,淡黄色固体溶解,混合液分层,该操作为萃取;
②进行分液(填操作名称),取所得上层清液继续进行实验;
③检验溶液中的阴离子(限选的试剂有:酚酞溶液、Ba(NO3)2溶液、AgNO3溶液、盐酸、稀HNO3、KMnO4溶液)
| 实验步骤 | 实验现象和结论 |
| 1.取少量溶液于试管中,滴入几滴KMnO4溶液 | KMnO4溶液颜色由紫色变绿色,说明溶液中大量存在SO32- |
| 2.另取少量溶液于试管中,加入2-3滴酚酞溶液 | 溶液颜色由无色变红,说明溶液中大量存在OH- |
| 3.另取少量溶液于试管中,加入足量1mol•L-1HNO3,再加入少量AgNO3溶液 | 仍有白色沉淀产生,说明溶液中大量存 |
8.一定条件下,下列能与CH3CH2COOH发生反应的物质是( )
①紫色石蕊溶液 ②乙醇 ③苯 ④金属钠 ⑤氧化铜 ⑥碳酸钙 ⑦氢氧化镁 ⑧乙烷.
①紫色石蕊溶液 ②乙醇 ③苯 ④金属钠 ⑤氧化铜 ⑥碳酸钙 ⑦氢氧化镁 ⑧乙烷.
| A. | ①③④⑤⑥⑦ | B. | ②③④⑤ | C. | ①②④⑤⑥⑦ | D. | 全部 |
5.下列说法中正确的是( )
| A. | 0.1 mol•L-1NH4Cl溶液的KW大于0.01mol?L-1NH4Cl溶液的KW | |
| B. | 当镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 | |
| C. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时,升高温度,反应速率v(H2)和H2的平衡转化率α(H2)均增大 | |
| D. | 水的离子积常数Kw 随着温度的升高而增大,说明水的电离是放热反应 |
6.除去括号内的杂质,填上适当的试剂和方法.
| 所需试剂 | 方法 | |
| 甲烷(乙烯) | 溴水 | 洗气 |
| 苯(酒精) | 水 | 分液 |
| 粗苯甲酸的提纯 | 水 | 重结晶 |
 ,⑦的电子式是
,⑦的电子式是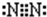 .
.