题目内容
 铁和铁的化合物在工业生产和日常生活中都有广泛的用途.请回答下列问题:
铁和铁的化合物在工业生产和日常生活中都有广泛的用途.请回答下列问题:(1)钢铁锈蚀是目前难以解决的现实问题,电化学腐蚀最为普遍.写出在潮湿空气中钢铁锈蚀时发生还原反应的电极反应式:
O2+4e-+2H2O=4OH-
O2+4e-+2H2O=4OH-
.铁锈的主要成分是Fe2O3?xH2O
Fe2O3?xH2O
(填写化学式),将生锈的铁屑放入H2SO4溶液中充分溶解后,在溶液中并未检测出Fe3+,用离子方程式说明原因:2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
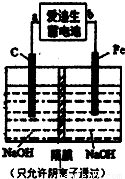
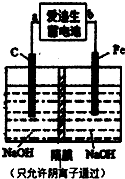
.(2)爱迪生蓄电池的反应式为:Fe+NiO2+2H2O
| ||
| 充电 |
①此装置中爱迪生蓄电池的负极是
a
a
(填“a”或“b”),该电池工作一段时间后必须充电,充电时生成NiO2的反应类型是氧化反应
氧化反应
.②写出在用电解法制取高铁酸钠时,阳极的电极反应式
Fe-6e-+8OH-=FeO42-+4H2O
Fe-6e-+8OH-=FeO42-+4H2O
.③你认为高铁酸钠作为一种新型净水剂的理由可能是
BC
BC
.A.高铁酸钠溶于水形成一种胶体,具有较强的吸附性
B.高铁酸钠具有强氧化性,能消毒杀菌
C.高铁酸钠在消毒杀菌时被还原生成Fe3+,水解产生氢氧化铁胶体能吸附悬浮杂质.
分析:(1)钢铁在潮湿的空气中发生吸氧腐蚀,正极上得电子发生还原反应;负极上铁失电子发生氧化反应,正极上得电子发生还原反应,二价铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁被氧化生成氢氧化铁,氢氧化铁失去部分水生成铁锈;铁和铁离子能发生氧化还原反应生成亚铁离子.
(2)①放电时,铁棒作负极,碳棒作正极,据此判断a的电极;失电子的物质发生氧化反应.
②铁失电子和氢氧根离子生成高铁酸根离子和水.
③高铁酸根离子有强氧化性,被还原生成的三价铁离子能发生生成胶体,胶体具有吸附性.
(2)①放电时,铁棒作负极,碳棒作正极,据此判断a的电极;失电子的物质发生氧化反应.
②铁失电子和氢氧根离子生成高铁酸根离子和水.
③高铁酸根离子有强氧化性,被还原生成的三价铁离子能发生生成胶体,胶体具有吸附性.
解答:解:(1)钢铁在潮湿的空气中发生吸氧腐蚀,正极上氧气得电子和水反应生成氢氧根离子O2+4e-+2H2O=4OH-;负极上铁失电子发生氧化反应,正极上发生的反应为O2+4e-+2H2O=4OH-,二价铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁被氧化生成氢氧化铁,氢氧化铁失去部分水生成铁锈,所以铁锈的成分是Fe2O3?xH2O;铁和铁离子能发生氧化还原反应生成亚铁离子2Fe3++Fe=3Fe2+,导致溶液中不存在铁离子.
故答案为:O2+4e-+2H2O=4OH-;Fe2O3?xH2O;2Fe3++Fe=3Fe2+.
(2)①放电时,铁作负极,碳棒作正极,所以放电时a是负极,b是正极;充电时,氢氧化镍失电子生成氧化镍,发生氧化反应.
故答案为:a;氧化反应.
②阳极上铁失电子和氢氧根离子反应生成高铁酸根离子和水,离子方程式为:Fe-6e-+8OH-=FeO42-+4H2O.
故答案为:Fe-6e-+8OH-=FeO42-+4H2O.
③高铁酸钠具有强氧化性,所以能杀菌消毒;高铁酸钠能被还原生成铁离子,铁离子能水解生成氢氧化铁胶体,胶体具有吸附性,能吸附悬浮杂质,所以能净水.
故选BC.
故答案为:O2+4e-+2H2O=4OH-;Fe2O3?xH2O;2Fe3++Fe=3Fe2+.
(2)①放电时,铁作负极,碳棒作正极,所以放电时a是负极,b是正极;充电时,氢氧化镍失电子生成氧化镍,发生氧化反应.
故答案为:a;氧化反应.
②阳极上铁失电子和氢氧根离子反应生成高铁酸根离子和水,离子方程式为:Fe-6e-+8OH-=FeO42-+4H2O.
故答案为:Fe-6e-+8OH-=FeO42-+4H2O.
③高铁酸钠具有强氧化性,所以能杀菌消毒;高铁酸钠能被还原生成铁离子,铁离子能水解生成氢氧化铁胶体,胶体具有吸附性,能吸附悬浮杂质,所以能净水.
故选BC.
点评:本题以安迪生电池为载体考查了原电池原电池和电解池原理,难度不大,明确高铁酸钠能作为一种新型净水剂的原理.

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案
相关题目
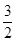 C(s)=
C(s)=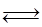 2Fe(s)+3CO2(g);工业上有16 t Fe2O3在200m3的容器中反应,l小时后测得Fe2O3的转化率为50%,则这段时间内CO的消耗速率为 mol/(L·h).
2Fe(s)+3CO2(g);工业上有16 t Fe2O3在200m3的容器中反应,l小时后测得Fe2O3的转化率为50%,则这段时间内CO的消耗速率为 mol/(L·h). Fe(OH)2+Ni(OH)2;高铁酸钠( Na2FeO4)是一种新型饮水消毒剂.用题29图装置可以制取少量高铁酸钠.
Fe(OH)2+Ni(OH)2;高铁酸钠( Na2FeO4)是一种新型饮水消毒剂.用题29图装置可以制取少量高铁酸钠.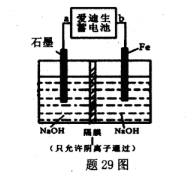
 C(s)=
C(s)=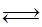 2Fe(s)+3CO2(g);工业上有16 t Fe2O3在200m3的容器中反应,l小时后测得Fe2O3的转化率为50%,则这段时间内CO的消耗速率为 mol/(L·h).
2Fe(s)+3CO2(g);工业上有16 t Fe2O3在200m3的容器中反应,l小时后测得Fe2O3的转化率为50%,则这段时间内CO的消耗速率为 mol/(L·h). Fe(OH)2+Ni(OH)2;高铁酸钠( Na2FeO4)是一种新型饮水消毒剂.用题29图装置可以制取少量高铁酸钠.
Fe(OH)2+Ni(OH)2;高铁酸钠( Na2FeO4)是一种新型饮水消毒剂.用题29图装置可以制取少量高铁酸钠.
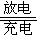 Fe(OH)2+Ni(OH)2;高铁酸酸钠(Na2FeO4)是一种新型净水剂.用下面装置可以制取少量高铁酸钠.
Fe(OH)2+Ni(OH)2;高铁酸酸钠(Na2FeO4)是一种新型净水剂.用下面装置可以制取少量高铁酸钠.