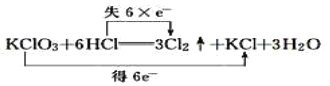
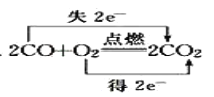
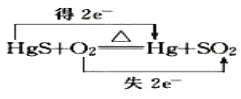
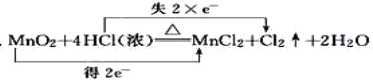��Ŀ����
����Ŀ��CuCl�㷺Ӧ���ڻ�����ӡȾ����ҵ��ij�о���ѧϰС�����ȷֽ�CuCl2��2H2O�Ʊ�CuCl�����������̽����
�����ϲ��ģ�
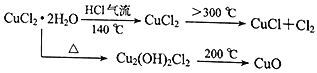
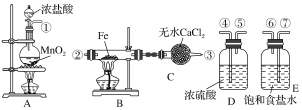
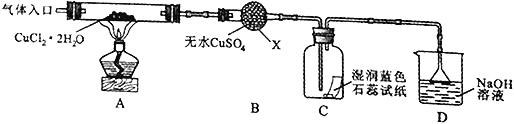
��ʵ��̽������С������ͼ��ʾװ�ý���ʵ�飨�г������ԣ���
��ش��������⣺
��1��ʵ��������Ⱥ�˳����a��_______________��e��������ı�ţ���
a�����װ�õ������Ժ����ҩƷ b��Ϩ��ƾ��ƣ���ȴ
c���ڡ�������ڡ���ͨ�����HCl d����ȼ�ƾ��ƣ�����
e��ֹͣͨ��HCl��Ȼ��ͨ��N2
��2����ʵ������У��۲쵽B�������ɰ�ɫ��Ϊ��ɫ��C����ֽ����ɫ�仯��_______��
��3��װ��D�з�����������ԭ��Ӧ�����ӷ���ʽ��________________��
��4����Ӧ������ȡ��CuCl��Ʒ����ʵ�飬�������к���������CuCl2��CuO���ʣ�����������Ϣ
����������CuCl2���������ԭ����________________��
����������CuO���������ԭ����________________��
���𰸡�c d b�ȱ�죬����ɫCl2+2OH-=Cl-+ClO-+H2O�ټ���ʱ�䲻����¶�ƫ�͢�ͨ��HCl��������
��������
��1������ʵ��Ҫ����Ϣ��֪�����ȼ��װ�õ������ԣ�����ҩƷ��Ӧ�ڡ�������ڡ���ͨ�������Ȼ��⣬�ٵ�ȼ�ƾ��Ƽ��ȣ�����Ӧ��ɺ���Ϩ��ƾ�����ȴ�����ֹͣͨ���Ȼ��⣬��ͨ������ȥװ���е��Ȼ������������ʵ��IJ���˳��Ϊ��a c d b e��
��2����ˮ����ͭ����Ӧ�����ɵ�ˮ��������������Ӧ�����ɵ��������ܱ���ˮ����ͭ���գ������������뵽Cװ�ã��������Ӵ���ʪ�����ɫʯ����ֽʱ��������ˮ��Ӧ��������ʹ����ᣬ����ʹ��ֽ�ȱ�죬��������ǿ�����ԣ�����ʹ��ɫʯ����ֽ��ɫ��
��3��D�е�����������Һ�������ն�����Ȼ������������ֹ��Ⱦ�����������������������Ʒ�ӦΪ������ԭ��Ӧ�����ӷ���ʽΪ: Cl2+2OH-=Cl-+ClO-+H2O��
��4���������Ϣ��֪������������CuCl2���������ԭ����û�б����¶��ڸ���300�������³�ַ�Ӧ��������ʱ�䲻����¶�ƫ�ͣ�����������CuO���������ԭ����ͨ���Ȼ���������㣬���¼���ʧˮ����������Cu2(OH)2Cl2�����ֽ���������ͭ��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�