题目内容
(1)在标准状况下,CO和CO2混合气体的质量为36g,体积为22.4L,则CO所占的体积为______L,混合气体中CO2的分子数为______.(2)在某未知体积的NaOH溶液中,经测定含有3.01×1023个OH-,则OH-的物质的量______mol,此溶液中,溶质的质量为______g,若用HCl中和此溶液,所需浓度2mol/L的HCl溶液体积______L.
【答案】分析:(1)(1)根据n=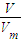 计算混合气体的物质的量,令混合气体中CO和CO2的物质的量分别为xmol、ymol,根据二者质量之和与物质的量之和列放出计算x、y的值,再根据V=nVm计算CO的体积,根据N=nNA计算CO2的分子数;
计算混合气体的物质的量,令混合气体中CO和CO2的物质的量分别为xmol、ymol,根据二者质量之和与物质的量之和列放出计算x、y的值,再根据V=nVm计算CO的体积,根据N=nNA计算CO2的分子数;
(2)根据n=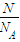 计算OH-的物质的量,根据m=nM计算NaOH的质量,氢氧化钠与HCl恰好完全中和,则n(HCl)=n(NaOH),再根据V=
计算OH-的物质的量,根据m=nM计算NaOH的质量,氢氧化钠与HCl恰好完全中和,则n(HCl)=n(NaOH),再根据V= 计算需要盐酸的体积.
计算需要盐酸的体积.
解答:解:(1)标准状况下,混合气体的物质的量为 =1mol,
=1mol,
令混合气体中CO和CO2的物质的量分别为xmol、ymol,则:
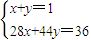
解得:x=0.5,y=0.5;
故CO的体积为0.5mol×22.4L/mol=11.2L,
CO2的分子数为0.5mol×NAmol-1=0.5NA,
故答案为:11.2;0.5NA;
(2)3.01×1023个OH-的物质的量为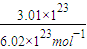 =0.5mol,故n(NaOH)=n(OH-)=0.5mol,所以氢氧化钠的质量为:0.5mol×40g/mol=20g,
=0.5mol,故n(NaOH)=n(OH-)=0.5mol,所以氢氧化钠的质量为:0.5mol×40g/mol=20g,
氢氧化钠与HCl恰好完全中和,则n(HCl)=n(NaOH)=0.5mol,需要盐酸的体积的体积为: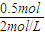 =0.25L,
=0.25L,
故答案为:0.5;20;0.25.
点评:本题考查物质的量的有关计算、混合物的有关计算等,比较基础,注意对基础知识的理解掌握,注意对公式的理解与运用.
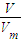 计算混合气体的物质的量,令混合气体中CO和CO2的物质的量分别为xmol、ymol,根据二者质量之和与物质的量之和列放出计算x、y的值,再根据V=nVm计算CO的体积,根据N=nNA计算CO2的分子数;
计算混合气体的物质的量,令混合气体中CO和CO2的物质的量分别为xmol、ymol,根据二者质量之和与物质的量之和列放出计算x、y的值,再根据V=nVm计算CO的体积,根据N=nNA计算CO2的分子数;(2)根据n=
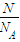 计算OH-的物质的量,根据m=nM计算NaOH的质量,氢氧化钠与HCl恰好完全中和,则n(HCl)=n(NaOH),再根据V=
计算OH-的物质的量,根据m=nM计算NaOH的质量,氢氧化钠与HCl恰好完全中和,则n(HCl)=n(NaOH),再根据V= 计算需要盐酸的体积.
计算需要盐酸的体积.解答:解:(1)标准状况下,混合气体的物质的量为
 =1mol,
=1mol,令混合气体中CO和CO2的物质的量分别为xmol、ymol,则:
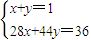
解得:x=0.5,y=0.5;
故CO的体积为0.5mol×22.4L/mol=11.2L,
CO2的分子数为0.5mol×NAmol-1=0.5NA,
故答案为:11.2;0.5NA;
(2)3.01×1023个OH-的物质的量为
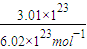 =0.5mol,故n(NaOH)=n(OH-)=0.5mol,所以氢氧化钠的质量为:0.5mol×40g/mol=20g,
=0.5mol,故n(NaOH)=n(OH-)=0.5mol,所以氢氧化钠的质量为:0.5mol×40g/mol=20g,氢氧化钠与HCl恰好完全中和,则n(HCl)=n(NaOH)=0.5mol,需要盐酸的体积的体积为:
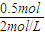 =0.25L,
=0.25L,故答案为:0.5;20;0.25.
点评:本题考查物质的量的有关计算、混合物的有关计算等,比较基础,注意对基础知识的理解掌握,注意对公式的理解与运用.

练习册系列答案
相关题目
下列关于气体摩尔体积的几种说法正确的是( )
| A、22.4 L任何气体的物质的量均为1 mol | B、标准状况下,1 mol物质的体积为22.4 L | C、H2、O2、N2、CO2组成的混合气体1 mol在标准状况下的体积约为22.4 L | D、在同温同压下,相同体积的任何气体单质所含分子数和原子数都相同 |
 (1)在标准状况下,气体A的密度为1.25g/L,气体B相对于氢气的密度为21,若8.96LA和B的混合气体的质量为13.44g,则混合物中A与B的体积比为
(1)在标准状况下,气体A的密度为1.25g/L,气体B相对于氢气的密度为21,若8.96LA和B的混合气体的质量为13.44g,则混合物中A与B的体积比为