题目内容
17.在氯化铵溶液中,离子浓度的关系正确的是( )| A. | c(NH4+)>c(Cl-)>c(H+)>c(OH-) | B. | c(NH4+)>c(H+)>c(Cl-)>c(OH-) | ||
| C. | c(Cl-)>c(NH4+)>c(H+)>c(OH-) | D. | c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
分析 氯化铵溶液中,铵根离子部分水解呈酸性,则c(H+)>c(OH-),根据电荷守恒可知:c(Cl-)>c(NH4+),由于盐类水解程度较小,所以c(NH4+)>c(H+),据此判断溶液中各离子浓度大小.
解答 解:氯化铵溶液中,铵根离子部分水解,呈酸性,则:c(H+)>c(OH-),根据电荷守恒c(Cl-)+c(OH-)=c(NH4+)+c(H+)可知:c(Cl-)>c(NH4+),由于盐类水解程度较小,所以c(NH4+)>c(H+),
则溶液中离子浓度大小顺序为:c(Cl-)>c(NH4+)>c(H+)>c(OH-),
故选C.
点评 本题考查了离子浓度大小比较,题目难度中等,明确电荷守恒、物料守恒及盐的水解原理为解答关键,注意熟练掌握判断离子浓度大小常用方法,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.用苯酚做下列实验,能成功的是( )
| A. | 与浓硫酸和浓硝酸混合液发生硝化反应 | |
| B. | 与乙醇发生酯化反应 | |
| C. | 在80℃的水中形成乳浊液 | |
| D. | 与福尔马林在沸水浴中便可发生缩聚反应制酚醛树脂 |
8.含有等物质的量的CH3COOH和CH3COONa的混合溶液中,下列说法正确的是( )
| A. | c(CH3COOH)+c(H+ )<c(OH-)+c(CH3COO-) | B. | c(H+ )+c(CH3COOH)=c(OH-)+c(CH3COO-) | ||
| C. | c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | D. | c(Na+)=c(CH3COOH)+c(CH3COO-) |
12.已知aX n+和bYm- 两种离子的电子层结构相同,则下列关系成立的是( )
| A. | a=b+n-m | B. | 离子半径Y m-<X n+ | ||
| C. | 原子序数Y>X | D. | 原子半径X>Y |
2.市场上有些人不顾诚信与道德,用假货欺骗消费者.针对下面一些生活现象,某同学相应地提出了自己的观点,你认为错误的是( )
| A. | 某消费者购买了一件标识为含毛量100%的羊毛衫--可从毛衣上抽取丝毛点燃,根据能否产生烧焦蛋白质的特殊气味来初步判断是不是含有羊毛 | |
| B. | 某广告称某八宝粥(含桂圆、红豆、糯米等)未加糖,最适合糖尿病人食用--本广告有误导行为,不加糖不等于不含糖,糖尿病人食用需慎重 | |
| C. | 工业酒精勾兑的假酒伤人事件屡禁不止,某经营者称是由于消费者饮用过度导致--事实,甲醇、乙醇都是醇,甲醇更易醉死人,饮用工业酒精要适量 | |
| D. | 某公司称为了轻松“减肥”,可采用不运动、不节食、不忌口的快速瘦身药物疗法--不科学.多运动,可增加体内脂肪消耗;平衡膳食结构,少吃油腻食物,可防止脂肪在体内堆积过多 |
9.已知:25°C时,Ksp〔Mg(OH)2〕=5.61×10-12,Ksp〔MgF2〕=7.42×10-11.下列说法正确的是( )
| A. | 25°C时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大 | |
| B. | 25°C时,在Mg(OH)2的悬浊液加入少量的NH4Cl固体,c(Mg2+)增大 | |
| C. | 25°C时,Mg(OH)2固体在20mL0.01 mol•L-1氨水中的Ksp比在20mL0.01mol•L-1NH4Cl溶液中的Ksp小 | |
| D. | 25°C时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2不可能转化为MgF2 |
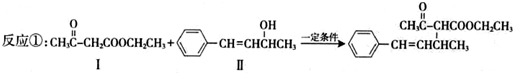
 .
.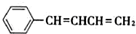 .
.