题目内容
16.某烃在标准状况下的密度为5.72g/L,现取1.28g该烃完全燃烧,将全部产物依次通入足量的浓硫酸和碱石灰,浓硫酸增重1.8g,碱石灰增重3.96g.请回答下列问题:(1)该烃的相对分子质量128.
(2)确定该烃的分子式C9H20.
(3)若该烃分子中含有6个甲基,则符合此条件的该烃的同分异构体有4种,任写一种的结构简式CH(CH3)2C(CH3)2CH(CH3)2.
分析 (1)摩尔质量=密度×气体摩尔体积,摩尔质量以g/mol作单位,数值上等于其相对分子质量;
(2)浓硫酸增重1.8g为生成的水的质量,碱石灰增重3.96g为燃烧生成CO2的质量,根据C原子、H原子守恒可计算出1.28g烃中C原子、H原子的物质的量,据此计算烃中C原子、H原子的个数比,即求出的实验式,再结合烃的相对分子质量确定其分子式;
(3)含有6个甲基就已经占了6个C和18个H,只剩下3个C和2个H,可以看作是丙烷中其中的六个H被6个甲基给取代了,由此分析解答.
解答 解:(1)烃的摩尔质量为:5.72g/L×22.4L/mol=128g/mol,摩尔质量以g/mol作单位,数值上等于其相对分子质量,所以该烃的相对分子质量为128,
故答案为:128;
(2)生成水的物质的量为:n(H2O)=$\frac{1.8g}{18g/mol}$=0.1mol,则:n(H)=2n(H2O)=0.1mol×2=0.2mol,生成CO2的物质的量为:n(CO2)=$\frac{3.96g}{44g/mol}$=0.09mol,则:n(C)=n(CO2)=0.09mol,烃中C原子、H原子的个数比为0.09mol:0.2mol=9:20,实验式为C9H20,该实验式中C原子与H原子的关系满足烷烃关系,实验式即是分子式,所以该烃的分子式为C9H20,故答案为:C9H20;
(3)丙烷的碳架结构为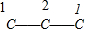 ,有两种氢分别是1号碳上6个氢,2号碳上2个氢,6个甲基取代1号碳上6个氢是一种;取代1号碳上5个氢,2号碳上1个氢是第二种,取代2号碳上两个氢,如果两个甲取代左1号碳,另两个甲基取代右1号碳上是第三种;取代2号碳上两个氢,如果三个甲取代左1号碳,另一个甲基取代右1号碳上是第由种,其中一种的结构简式为CH(CH3)2C(CH3)2CH(CH3)2,故答案为:4;CH(CH3)2C(CH3)2CH(CH3)2.
,有两种氢分别是1号碳上6个氢,2号碳上2个氢,6个甲基取代1号碳上6个氢是一种;取代1号碳上5个氢,2号碳上1个氢是第二种,取代2号碳上两个氢,如果两个甲取代左1号碳,另两个甲基取代右1号碳上是第三种;取代2号碳上两个氢,如果三个甲取代左1号碳,另一个甲基取代右1号碳上是第由种,其中一种的结构简式为CH(CH3)2C(CH3)2CH(CH3)2,故答案为:4;CH(CH3)2C(CH3)2CH(CH3)2.
点评 本题考查有机物分子式的确定,题目难度中等,注意掌握常见的有机物分子式的确定方法,明确根据质量守恒定律确定有机物的分子式的方法.

| A. | 将乙酸乙酯与H218O混合后,用稀硫酸作催化剂,借以判断乙酸乙酯水解时分子中共价键的断裂情况,该方法应称为同位素示踪法 | |
| B. | 相对分子质量的测定常用质谱仪,分子结构测定方法主要是用红外光谱等 | |
| C. | C6H5-OH能与浓溴水生成三溴苯酚,甲苯却不能与浓溴水反应,说明苯酚分子中由于苯环影响,使羟基上H原子变得活泼 | |
| D. | 某有机物C分子式为C11H14O2,其1H-NMR图谱如图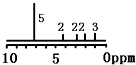 (峰右侧或上面的数字表示H的个数,且知:7.2ppm(5H)为苯基),可推测该有机物可能为 (峰右侧或上面的数字表示H的个数,且知:7.2ppm(5H)为苯基),可推测该有机物可能为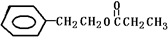 |
(1)要提高CO的转化率,可以采取的措施是df.
a.升温 b.加入催化剂 c.增加CO的浓度
d.充入H2 e.充入惰性气体 f.分离出甲醇
(2)在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温恒容,测得反应达到平衡时的有关数据如表:
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1mol CO、2mol H2 | 1mol CH3OH | 2mol CH3OH | |
| 平衡 时数 据 | CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的热量变化 | a kJ | b kJ | c kJ | |
| 体系压强(Pa) | p1 | p2 | p3 | |
| 反应物转化率 | α1 | α2 | α3 | |
A.2c1>c3 B.a+b<90.8 C.2p2<p3 D.α1+α3<1.
| A. | 该元素可能有放射性 | |
| B. | 该元素位于元素周期表中的第IIA族 | |
| C. | 其中子数与质子数之差为165 | |
| D. | 其原子质量是12C原子质量的277倍 |
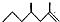 (2,4-二甲基-1-庚烯),
(2,4-二甲基-1-庚烯),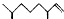 (3,7-二甲基-1-辛烯),家蚕的信息素为:CH3(CH2)2CH=CHCH=CH(CH2)8CH3.下列说法正确的是( )
(3,7-二甲基-1-辛烯),家蚕的信息素为:CH3(CH2)2CH=CHCH=CH(CH2)8CH3.下列说法正确的是( )| A. | 2,4-二甲基-1-庚烯与l-庚烯互为同分异构体 | |
| B. | 家蚕信息素与1molBr2加成产物只有3种 | |
| C. | 以上三种信息素均不能使溴的四氯化碳褪色 | |
| D. | 以上三种信息素都是乙烯的同系物 |
| A. | n+1 | B. | n+2 | C. | n+3 | D. | n+5 |
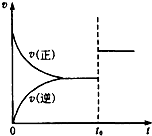 可逆反应aX(g)+bY(g)?cZ(g),在一定温度下的密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(v)和时间(t)的关系如图所示.下列说法中正确的是( )
可逆反应aX(g)+bY(g)?cZ(g),在一定温度下的密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(v)和时间(t)的关系如图所示.下列说法中正确的是( )| A. | 若a+b=c,则t0时只增大了反应物的浓度 | |
| B. | 若a+b=c,则t0时只升高了温度 | |
| C. | 若a+b≠c,则t0时只增大了容器的压强 | |
| D. | 若a+b≠c,则t0时只加入了催化剂 |
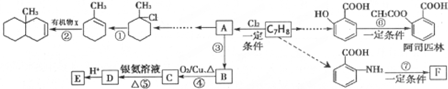
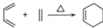
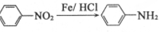 (苯胺,易被氧化)
(苯胺,易被氧化)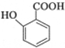 可选用的试剂有(填标号).a.FeCl3溶液 b.浓溴水 c.Na D.NaHCO3溶液
可选用的试剂有(填标号).a.FeCl3溶液 b.浓溴水 c.Na D.NaHCO3溶液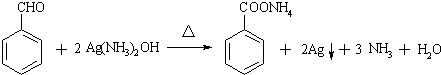 ;
;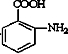 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$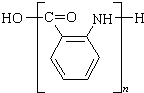 +(n-1)H2O.
+(n-1)H2O.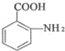 的合成路线流程图(无机试剂任用)
的合成路线流程图(无机试剂任用)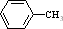 $→_{△}^{浓硫酸、浓硝酸}$
$→_{△}^{浓硫酸、浓硝酸}$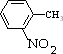 $\stackrel{酸性高锰酸钾溶液}{→}$
$\stackrel{酸性高锰酸钾溶液}{→}$ $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$