题目内容
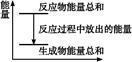
(1)1mol氢气在氯气中充分燃烧生成氯化氢气体时放出184.6 kJ的热量,试写出对应的热化学方程式 。标准状况下11.2L氢气在氯气中充分燃烧放出的热量是 kJ。
(2)A(g)+B(g) C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。
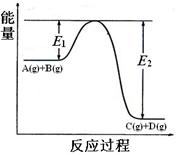
①反应物A(g)和B(g)具有的总能量 (填大于、小于、等于)生成物C(g)和D(g)具有的总能量。
②该反应是_______反应(填吸热、放热),△H= (用E1和E2表示)。
③稳定性:反应物 生成物(填大于、小于、等于)。
(2)A(g)+B(g)
 C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。
①反应物A(g)和B(g)具有的总能量 (填大于、小于、等于)生成物C(g)和D(g)具有的总能量。
②该反应是_______反应(填吸热、放热),△H= (用E1和E2表示)。
③稳定性:反应物 生成物(填大于、小于、等于)。
(1) H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6 kJ?mol-1 。 92.3 kJ。
(2)① 大于 ;②放热,△H=E1-E2 ③ 小于
(2)① 大于 ;②放热,△H=E1-E2 ③ 小于
试题分析:(1)1mol氢气在氯气中充分燃烧生成氯化氢气体时放出184.6 kJ的热量,则该反应的热化学方程式是H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6 kJ/mol。标准状况下11.2L氢气的物质的量是0.5mol,在氯气中充分燃烧放出的热量是184.6 kJ/mol×0.5mol=92.3kJ。
(2)①根据图像可知,反应物的总能量高于生成物的总能量,所以反应是放热反应。则反应物A(g)和B(g)具有的总能量大于生成物C(g)和D(g)具有的总能量。
②该反应是反应放热反应,△H=E1-E2。
③反应物的总能量高,所以稳定性是反应物小于生成物的。
点评:该题是中等难度试题的考查,主要是考查学生对热化学方程式书写以及反应热计算的熟悉了解程度,旨在巩固学生的基础,提高学生的应试能力,有利于调动学生的学习兴趣和学习积极性。

练习册系列答案
相关题目

 ,下列说法正确的是 。
,下列说法正确的是 。 2SO3(g) ΔH=-Q kJ·mol-1 (Q>0),下列说法正确的是
2SO3(g) ΔH=-Q kJ·mol-1 (Q>0),下列说法正确的是 
 2C(g)在反应过程中C的物质的量n(C)随着时间变化关系如图⑶所示,现从t1时间开始对反应体系升高温度,n(C)的变化如图qb所示。则:
2C(g)在反应过程中C的物质的量n(C)随着时间变化关系如图⑶所示,现从t1时间开始对反应体系升高温度,n(C)的变化如图qb所示。则: ZnSO4 + H2 的化学反应(反应放热),下列叙述一定正确的是
ZnSO4 + H2 的化学反应(反应放热),下列叙述一定正确的是