题目内容
【题目】A、B、C、D、E四种元素,它们原子的核电荷数均小于18,且依次递增,A原子核内仅有一个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等;D的最外层电子数是次外层电子数的3倍;E的单质是用途最广泛的半导体材料。试推断它们各是什么元素并回答下列问题:
(1)写出它们的元素符号:A________,B________,C________,D________,E________。
(2)B、C、D的气态氢化物的稳定性由大到小的顺序为__________(用化学式表示)
(3)画出D的离子结构示意图________。
(4)用一个方程式证明B、E的非金属性的强弱_______________。
(5)写出E的最高价氧化物的一种用途:_________。
(6)由这五种元素组成的三核10电子的分子为________,四核10电子的分子是________。由这五种元素组成的四核18电子的分子为________,五核18电子的分子是________。
【答案】H C N O Si H2O>NH3>CH4 ![]() Na2SiO3+H2O+CO2=H2SiO3↓+Na2CO3 制光导纤维(或制玻璃) H2O NH3 H2O2 SiH4
Na2SiO3+H2O+CO2=H2SiO3↓+Na2CO3 制光导纤维(或制玻璃) H2O NH3 H2O2 SiH4
【解析】
有A、B、C、D、E五种元素,它们原子的核电荷数依次递增且均小于18,A原子核内仅有1个质子,A应为H元素;D原子有两个电子层,最外层电子数是次外层电子数的3倍,最外层电子数为6,则D为O元素;B原子的电子总数与D原子的最外层电子数相等,则B为C元素;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等,C原子最外层电子数=1+4=5,且C的原子序数小于D,所以C是N元素;E的单质是用途最广泛的半导体材料,为Si元素,以此解答该题。
根据上述分析可知,
(1)A为H元素,B为C元素,C为N元素,D为O元素,E为Si元素;
(2)同周期元素原子的非金属性从左到右依次增强,气态氢化物的稳定性依次增强,因C、N、O的非金属性依次增强,故其气态氢化物的稳定性由大到小的顺序为H2O>NH3>CH4;
(3)D为O元素,核电荷数为8,其离子的结构示意图为:![]() ;
;
(4)C的非金属性比Si的强,可根据强酸制备弱酸的原理,结合其最高价氧化物对应水化物的酸性来判断,用化学方程式表示为:Na2SiO3+H2O+CO2=H2SiO3↓+Na2CO3;
(5)E的最高价氧化物为二氧化硅,可制光导纤维或制玻璃;
(6)A为H、B为C、C为N、D为O元素,由这四种元素组成的三核10电子的化合物为水,其分子式为:H2O;形成的四核10电子的分子是氨气,分子式为:NH3,
故答案为:H2O;NH3;
(7)水为三核10电子的分子,其化学式为H2O;氨气为四核10电子的分子,其化学式为:NH3;过氧化氢为四核18电子的分子,其化学式为:H2O2;氢化硅为五核18电子的分子,其化学式为:SiH4。

 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案【题目】温度分别为T1和T2时,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)![]() 2Z(g),一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g),一段时间后达到平衡,反应过程中测定的数据如下表:
温度/K | t/min | t1 | t2 | t3 | t4 |
T1 | n(Y)/mol | 0.14 | 0.12 | 0.10 | 0.10 |
T2 | n(Y)/mol | 0.13 | 0.09 | 0.08 |
下列说法正确的是( )
A. 该反应的正反应为放热反应
B. T2温度下此反应的平衡常数K=4
C. 温度为T1时,0~t1时间段的平均速率υ(Z)=2.0×10-3mol·L-1·min-1
D. 在T1下平衡后,保持其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
【题目】研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:Fe2O3(s)+ 3C(s)=2Fe(s)+ 3CO(g) ΔH 1=+489.0 kJ·mol-1
C(s) +CO2(g)=2CO(g) ΔH 2 =+172.5 kJ·mol-1。则CO还原Fe2O3(s)的热化学方程式为_________________________________________________。
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液)。写出该电池的负极反应式:__________________________________________________。
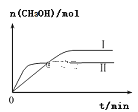
(3)①CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),测得CH3OH的物质的量随时间的变化如图。①曲线I、Ⅱ对应的平衡常数大小关系为KⅠ___________________KⅡ(填“>”或“=”或“<”)。
CH3OH(g)+H2O(g),测得CH3OH的物质的量随时间的变化如图。①曲线I、Ⅱ对应的平衡常数大小关系为KⅠ___________________KⅡ(填“>”或“=”或“<”)。
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
容 器 | 甲 | 乙 |
反应物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
若甲中平衡后气体的压强为开始的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为______________________。
③一定温度下,此反应在恒压容器中进行,能判断该反应达到化学平衡状态的依据是______________。
a.容器中压强不变 b.H2的体积分数不变 c.c(H2)=3c(CH3OH)
d.容器中密度不变 e.2个C=O断裂的同时有3个H-H断裂
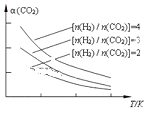
(4)将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g) + 6H2(g)![]() CH3OCH3(g) + 3H2O(g)。已知一定条件下,该反应中CO2的平衡转化率随温度、投料比[n(H2) / n(CO2)]的变化曲线如图,若温度不变,提高投料比n(H2)/n(CO2),则K将__________;该反应△H_________0(填“>”、“<”或“=”)。
CH3OCH3(g) + 3H2O(g)。已知一定条件下,该反应中CO2的平衡转化率随温度、投料比[n(H2) / n(CO2)]的变化曲线如图,若温度不变,提高投料比n(H2)/n(CO2),则K将__________;该反应△H_________0(填“>”、“<”或“=”)。