��Ŀ����
����Ŀ����ͼ��ʵ�����Ʊ��������֤�������ʵ�װ��ͼ�� 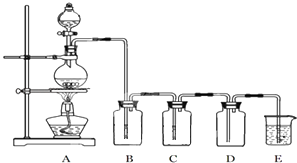
��1����������ͼװ���Ʊ������������������װ��A�з�Ӧ�Ļ�ѧ����ʽΪ �� װ��Bʢ����װ��C���Լ��������� ��
��2����������ͼװ��ʵ��̼��Ũ����ķ�Ӧ��������������֤�� ��װ��B��C��D��E�зֱ�װ��Ʒ����Һ������KMnO4��Һ��Ʒ����Һ������ʯ��ˮ����Dװ����Ʒ����Һ�������� �� ֤����������CO2�������� ��
����֤��SO2���������ԣ�ͬʱ֤��̼������Աȹ����ǿ��B��C��D�зֱ�װ��Na2S��Һ����������KMnO4��Һ��Ʒ����Һ��
��B�е����� �� F��Ӧ������Һ��E�з�����Ӧ�����ӷ���ʽΪ ��
���𰸡�
��1��MnO2+4HCl ![]() MnCl2+Cl2��+2H2O������ʳ��ˮ������Cl2
MnCl2+Cl2��+2H2O������ʳ��ˮ������Cl2
��2����֤SO2�Ƿ������ Dװ����Ʒ�첻��ɫ,Eװ�����а�ɫ�������л�ɫ������ Na2SiO3�� SiO32��+2H2O+CO2=H4SiO4��+CO32��
���������⣺��1����������ͼװ���Ʊ���������������������ö������̺�Ũ�����ڼ����������Ʊ�����Ӧ�Ļ�ѧ����ʽΪMnO2+4HCl ![]() MnCl2+Cl2��+2H2O��B���ڳ���HCl��C���ڸ��DΪ�����ռ�װ�ã�EΪβ������װ�ã�
MnCl2+Cl2��+2H2O��B���ڳ���HCl��C���ڸ��DΪ�����ռ�װ�ã�EΪβ������װ�ã�
���Դ��ǣ�MnO2+4HCl ![]() MnCl2+Cl2��+2H2O������ʳ��ˮ������Cl2����2��̼��Ũ������ȷ�Ӧ���ɶ�����̼�����������ˮ������C+2H2SO4��Ũ��
MnCl2+Cl2��+2H2O������ʳ��ˮ������Cl2����2��̼��Ũ������ȷ�Ӧ���ɶ�����̼�����������ˮ������C+2H2SO4��Ũ�� ![]() CO2��+SO2��+2H2O��
CO2��+SO2��+2H2O��
��װ��B��C��D��E�зֱ�װ��Ʒ����Һ������KMnO4��Һ��Ʒ����Һ������ʯ��ˮ����Dװ����Ʒ����Һ����������֤���������Ƿ��������Һ��ȫ���գ�֤����������CO2��������Dװ����Ʒ�첻��ɫ��Eװ�����а�ɫ������
���Դ��ǣ���֤SO2�Ƿ������Dװ����Ʒ�첻��ɫ��Eװ�����а�ɫ������
����֤��SO2���������ԣ�ͨ��װ��B�е�Na2S��Һ��֤��������������Ʒ�Ӧ�������ʣ���Һ�б���ǣ�֤��̼������Աȹ����ǿ����ͨ�����������Һ��ȥ�����������ͨ��Ʒ����Һ������������Ƿ������������ͨ����������Һ���ɰ�ɫ����֤��̼������Աȹ����ǿ��װ��E��Ϊ��������Һ��B���г���ΪS��������̼��������Һ��Ӧ���ɰ�ɫ�������ᣬ��Ӧ�����ӷ���ʽΪ��SiO32��+2H2O+CO2=H4SiO4��+CO32����
���Դ��ǣ��л�ɫ������Na2SiO3��SiO32��+2H2O+CO2=H4SiO4��+CO32����

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�

