题目内容
【题目】
(1)1909年化学家哈伯在实验室首次合成了氨,2007年化学家格哈德埃特尔在哈伯研究所证实了N2与H2在固体催化剂表面合成氨的反应过程。示意图如下(![]()
![]()
![]() 分别表示N2、H2、NH3):
分别表示N2、H2、NH3):
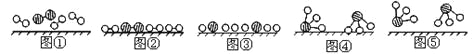
图②表示N2、H2被吸附在催化剂表面,图⑤表示生成的NH3离开催化剂表面,则图③表示 。
(2)NaNO2是一种食品添加剂(有毒性,市场上常误与食盐混淆)。酸性KMnO4溶液与NaNO2反应的离子方程式是:MnO4-+NO2-+X![]() Mn2++NO3-+H2O(未配平),X表示的粒子是 。酸性高锰酸钾 (“能”或“不能”)鉴别食盐中是否存在NaNO2,理由是___________________
Mn2++NO3-+H2O(未配平),X表示的粒子是 。酸性高锰酸钾 (“能”或“不能”)鉴别食盐中是否存在NaNO2,理由是___________________
【答案】(1)在催化剂表面N2、H2分子的化学键断裂生成N原子和H原子(2分)
(2)H+不能 酸性高锰酸钾溶液既能氧化Cl-又能氧化NO2-(4分)
【解析】试题解析:(1)图②表示N2、H2被吸附在催化剂表面,图⑤表示生成的NH3离开催化剂表面,则图③表示在催化剂表面N2、H2分子的化学键断裂生成N原子和H原子;(2)MnO4-+NO2-+X![]() Mn2++NO3-+H2O;根据原子守恒规律:X表示的粒子是H+;不能;原因:酸性高锰酸钾溶液具有强氧化性,既能氧化食盐中的NaNO2,又能氧化食盐中氯离子;
Mn2++NO3-+H2O;根据原子守恒规律:X表示的粒子是H+;不能;原因:酸性高锰酸钾溶液具有强氧化性,既能氧化食盐中的NaNO2,又能氧化食盐中氯离子;
考点: 工业合成氨气反应过程,氯化钠和亚硝酸钠的鉴别;

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目