题目内容
下列变化需要加入适当的氧化剂才能完成的是( )
| A、CuO→Cu |
| B、Fe→FeCl3 |
| C、H2SO4→SO2 |
| D、HNO3→N2O |
考点:氧化还原反应
专题:氧化还原反应专题
分析:需要加入适当的氧化剂才能完成,则选项中为还原剂的氧化反应,还原剂中某元素的化合价升高,以此来解答.
解答:
解:A.Cu元素的化合价降低,需要加还原剂,故A不选;
B.Fe元素的化合价升高,需要加氧化剂,故B选;
C.S元素的化合价降低,需要加还原剂,故C不选;
D.N元素的化合价降低,需要加还原剂,故D不选;
故选B.
B.Fe元素的化合价升高,需要加氧化剂,故B选;
C.S元素的化合价降低,需要加还原剂,故C不选;
D.N元素的化合价降低,需要加还原剂,故D不选;
故选B.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化反应的考查,注意从化合价角度分析,题目难度不大.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案
相关题目
下列四图中,曲线变化情况与所给反应(a、b、c、d均大于0)相对应的是( )
A、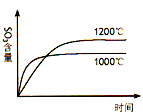 2SO2(g)+O2(g)?2SO3(g)△H=-akJ?mol-1 |
B、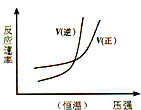 N2(g)+3H2(g)?NH3(g)△H=-bkJ?mol-1 |
C、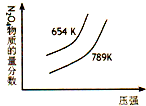 N2O4(g)?2NO2(g)△H=+ckJ?mol-1 |
D、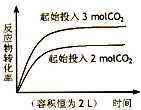 CO2(g)+C(s)?2CO(g)△H=+dkJ?mol-1 |
将紫色石蕊试液滴入NaOH溶液中,溶液变蓝色,再通入氯气,溶液由蓝色先变成红色,最后颜色慢慢退去,其原因是( )
①氯气有漂白性 ②氯气与NaOH溶液反应 ③氯气的水溶液呈酸性 ④次氯酸有漂白性 ⑤氯化钠有漂白性.
①氯气有漂白性 ②氯气与NaOH溶液反应 ③氯气的水溶液呈酸性 ④次氯酸有漂白性 ⑤氯化钠有漂白性.
| A、①④ | B、②③④ |
| C、①②③ | D、④⑤ |
化学与社会、环境、生活密切相关.下列说法正确的是( )
| A、食盐、食醋和味精是常用的食品添加剂,其主学成分均属钠盐 |
| B、SO2、C02、NO2均被列入我国空气质量报告的指标 |
| C、青铜是我国使用最早的合金 |
| D、家用84消毒液可用来漂白衣物,为了增强其漂白效果,使用时可加浓盐酸 |
已知273K时有反应:4C(g)?2A(g)+B(g)△H=-Q kJ/mol在相同温度条件下,向一密闭容器中通入4mol C达到平衡时放出的热量为Q1,向另一容积相同的密闭容器中通入2mol C达到平衡时,放出的热量为Q2,则Q1、Q2满足的关系是( )
A、Q2<
| ||
B、Q2=
| ||
| C、Q2<Q1=Q | ||
| D、Q1=Q2<Q |
下列有关说法正确的是( )
| A、一定条件下,使用催化剂能加快反应速率但不能改变平衡转化率 |
| B、氢氧燃料电池的能量转换形式仅为化学能转化为电能 |
| C、升高温度水的离子积常数减小 |
| D、根据能量守恒定律,反应物的总能量一定等于生成物的总能量 |
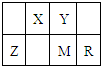 五种短周期元素(用字母表示)在周期表中的相对位置如图,其中Y的单质在空气中含量最高.下列判断正确的是( )
五种短周期元素(用字母表示)在周期表中的相对位置如图,其中Y的单质在空气中含量最高.下列判断正确的是( )| A、最高价氧化物的水化物的酸性:X>Y |
| B、气态氢化物稳定性:Y<M |
| C、R的氧化物的水化物是离子化合物 |
| D、Z、M、R的原子半径依次减小,最高化合价依次升高 |
“细节决定成败”对于下列实验细节处理正确的是( )
| A、实验室制氢气:为了加快反应速率,向稀H2SO4滴加少量CuSO4溶液 |
| B、钠与水的反应:取绿豆大小的金属钠放入烧杯,再滴入两滴酚酞试液,最后加入水 |
| C、配置0.10mol/L NaOH溶液:称取0.4g NaOH放入100mL容量瓶,加水至100mL |
| D、配置FeCl2溶液:称取一定量的FeCl2固体,加水溶解,在加入稀盐酸酸化 |
下列反应中离子方程式的书写正确的是( )
| A、向Na2CO3溶液中逐滴滴加盐酸:2H++CO32-═CO2↑+H2O |
| B、向FeCl3溶液中通入H2S气体:Fe3++H2S═Fe2++S↓+2H+ |
| C、向碳酸氢钠溶液中滴加过量的澄清石灰水:HCO3-+Ca2++OH-═CaCO3↓+H2O |
| D、浓度均为0.1mol/L的硫酸氢铵与氢氧化钠两种溶液等体积混合:NH4++HSO4-+2OH-═SO42-+NH3↑+2H2O |