题目内容
A、B是短周期第ⅦA族元素,元素A的非金属性比B强,下列说法正确的
A.NaA、NaB的晶体都是离子晶体
B.单质A可把B从NaB的溶液中置换出来
C.HA比HB沸点高的原因是1mol HA分子中H-A键断裂时吸收的能量比1mol HB分子中H-B键断裂时需要吸收的能量多
D.常温下,NaA、NaB溶液的pH均大于7
A.NaA、NaB的晶体都是离子晶体
B.单质A可把B从NaB的溶液中置换出来
C.HA比HB沸点高的原因是1mol HA分子中H-A键断裂时吸收的能量比1mol HB分子中H-B键断裂时需要吸收的能量多
D.常温下,NaA、NaB溶液的pH均大于7
A
由题意可知A为F元素,B为CL元素;所以
A正确,NaF、NaCL晶体均为离子晶体;B错,将F2通入NaBr溶液中反应的方程式为:
 ;C错,HA比HB沸点高的原因是:HF分子间存在氢键;D错,NaF为强碱弱酸盐,溶液显碱性,NaCL为强酸强碱盐,溶液显中性;
;C错,HA比HB沸点高的原因是:HF分子间存在氢键;D错,NaF为强碱弱酸盐,溶液显碱性,NaCL为强酸强碱盐,溶液显中性;
A正确,NaF、NaCL晶体均为离子晶体;B错,将F2通入NaBr溶液中反应的方程式为:
 ;C错,HA比HB沸点高的原因是:HF分子间存在氢键;D错,NaF为强碱弱酸盐,溶液显碱性,NaCL为强酸强碱盐,溶液显中性;
;C错,HA比HB沸点高的原因是:HF分子间存在氢键;D错,NaF为强碱弱酸盐,溶液显碱性,NaCL为强酸强碱盐,溶液显中性;
练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案
相关题目
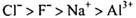
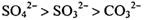

 的说法正确的是
的说法正确的是


 _______________。
_______________。