��Ŀ����
������һ����Ҫ�Ļ�����Ʒ����������Ρ����صȵ�ԭ�ϡ���ҵ�ϳɰ��ķ�Ӧ����:N2(g) +3H2(g)  2NH3(g) ��H=һ92. 4 KJ��mol-1
2NH3(g) ��H=һ92. 4 KJ��mol-1
��1��2NH3(g) N2(g) +3H2(g)�ں����ܱ������дﵽƽ��ı�־��
N2(g) +3H2(g)�ں����ܱ������дﵽƽ��ı�־��
�ٵ�λʱ��������3n mol H2:ͬʱ����2n mol NH3����NH3��N2��H2��ʾ��Ӧ���ʱ�Ϊ2��1��3 �ۻ��������ܶȲ��ٸı� �ܻ������ѹǿ���ٸı� �ݻ������ƽ����Է����������ٸı�
��2����ҵ�ϳ���CO2��NH3ͨ�����·�Ӧ�ϳ�����[CO(NH2)2]��
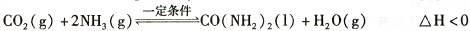
t��ʱ�����ݻ��㶨Ϊ2L���ܱ������м���0.10 molCO:��0. 40 molNH3 ,70 min��ʼ�ﵽƽ�⡣��Ӧ��CO2 ( g)�����ʵ�����ʱ��仯���±���ʾ:
��20 minʱ������(CO2 )_����������80 minʱ������(H2O)(�>������=����<��)��
����100 minʱ�����������������䣬���������г���0. 050 mo1CO2��0. 20 molNH3�����½���ƽ���CO2��ת������ԭƽ����Ƚ�_ (����������䡱��С��)��
���������淴Ӧ��ƽ�ⳣ��Ϊ_ (������λС��)��
�ܸ��ݱ���������ͼ���л��Ƴ���t����NH3��ת������ʱ��仯��ͼ��;����������������;��(t+10)������ȷ��ͼ������� (��ͼ���еġ�A����B��)��

��ͼ����ʾװ��(����������Ϊ���Ե缫)�����ڵ�����ء�CO(NH2)2���ļ�����Һ��ȡ��������װ���������ĵ缫��ӦʽΪ �����������ռ�������22. 4L(��
��)�������ĵ�����Ϊ g(����������ܽ�)��
 2NH3(g) ��H=һ92. 4 KJ��mol-1
2NH3(g) ��H=һ92. 4 KJ��mol-1��1��2NH3(g)
 N2(g) +3H2(g)�ں����ܱ������дﵽƽ��ı�־��
N2(g) +3H2(g)�ں����ܱ������дﵽƽ��ı�־���ٵ�λʱ��������3n mol H2:ͬʱ����2n mol NH3����NH3��N2��H2��ʾ��Ӧ���ʱ�Ϊ2��1��3 �ۻ��������ܶȲ��ٸı� �ܻ������ѹǿ���ٸı� �ݻ������ƽ����Է����������ٸı�
| A���٢ۢ� | B���٢ڢܢ� | C���٢ܢ� | D���ڢۢ� |
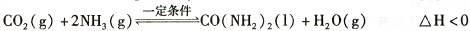
t��ʱ�����ݻ��㶨Ϊ2L���ܱ������м���0.10 molCO:��0. 40 molNH3 ,70 min��ʼ�ﵽƽ�⡣��Ӧ��CO2 ( g)�����ʵ�����ʱ��仯���±���ʾ:
| ʱ�䣯min | ��0 | 30 | 70 | 80 | 100 |
| n(CO2) ��mol | 0.10 | 0.060 | 0.040 | 0.040 | 0.040 |
��20 minʱ������(CO2 )_����������80 minʱ������(H2O)(�>������=����<��)��
����100 minʱ�����������������䣬���������г���0. 050 mo1CO2��0. 20 molNH3�����½���ƽ���CO2��ת������ԭƽ����Ƚ�_ (����������䡱��С��)��
���������淴Ӧ��ƽ�ⳣ��Ϊ_ (������λС��)��
�ܸ��ݱ���������ͼ���л��Ƴ���t����NH3��ת������ʱ��仯��ͼ��;����������������;��(t+10)������ȷ��ͼ������� (��ͼ���еġ�A����B��)��

��ͼ����ʾװ��(����������Ϊ���Ե缫)�����ڵ�����ء�CO(NH2)2���ļ�����Һ��ȡ��������װ���������ĵ缫��ӦʽΪ �����������ռ�������22. 4L(��
��)�������ĵ�����Ϊ g(����������ܽ�)��
21.��1��C; ��2����>;������76.53��B��CO(NH2)2 -6e- + 8OH- = CO32- + N2 +6H2O
��������� ��1�� �ٵ�λʱ��������3n mol H2:ͬʱ����2n mol NH3,�൱��ͬһ���ʵ����淴Ӧ������ȣ���ȷ������NH3��N2��H2��ʾ��Ӧ���ʱ�Ϊ 2��1��3 ��������ƽ���û��ƽ�������ϵ�����������ۻ��������ܶȲ��ٸı䣬�������������������У������������䣬�����ܶ�һֱ���䣬������Ϊƽ���ж����ݣ����� �����������ʵ�����Ӧǰ�����ı䣬�������ѹǿ���ٸı�ʱ������Ϊ�ж����ݣ���ȷ�� �ݻ������ƽ����Է��������������������������ʵ������������䵫�����ʵ��������ı䣬�����ٸı�ʱ˵���ﵽƽ�⣬��ȷ����2��������û�дﵽƽ�⣬ƽ����������Ӧ����ʱ���У�����20 minʱ����(CO2 )Ӧ�ô���80 minʱ������100 minʱ�����������������䣬���������г���0. 050 mo1CO2��0. 20 molNH3���൱�ڿ�ʼ�����˷�Ӧ������0. 150 mo1CO2��0. 60 molNH3�������Ǻ����������൱��������ѹǿƽ�����ƣ����½���ƽ���CO2��ת������ԭƽ����Ƚ����۸�����̬�����Լ���Ϊ��

��ʼ��0.1 0.4 0 0
ת����0.06 0.12 0.06 0.06
ƽ�⣺0.04 0.28 0.06 0.06
�������淴Ӧ��ƽ�ⳣ��ΪK=0.03*0.03/0.142*0.02=76.53������t�浽(t+10)���������¶�ƽ�������ƶ���������ת���ʽ��ͣ���ѡ��ȷ��ͼ�������B�����ڵ�����������ӦӦ����ʧ���ӵģ�Ӧ�����ɵ������ʵ缫��ӦΪCO(NH2)2 -6e- + 8OH- = CO32- + N2 +6H2O���������������ɣ����ݵ����غ㣬����������1mol����ʱ����Ӧ����3mol�������ɣ�������1mol��������ʱ��������е���0.25mol,��������0.25mol,�������15g��

��ϰ��ϵ�д�
�����Ŀ
 4NO(g)��6H2O(g)����H����905.5 kJ��mol��1
4NO(g)��6H2O(g)����H����905.5 kJ��mol��1
 2NH3(g) ��92.4 kJ������ʱ����ϵ�и�����Ũ����ʱ��仯��������ͼʾ������˵���������
2NH3(g) ��92.4 kJ������ʱ����ϵ�и�����Ũ����ʱ��仯��������ͼʾ������˵���������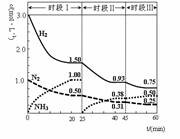
 2C��g��+ D��s�� ��5 min��ﵽƽ�⡣ƽ��ʱAΪ1.6mol���ų�������ΪQ����t0ʱ�̣�����ƽ����ϵ�з�����ķ�֮һ�Ļ�����壬��ƽ����ϵ��c(A)Ϊ0.6mol��L��
2C��g��+ D��s�� ��5 min��ﵽƽ�⡣ƽ��ʱAΪ1.6mol���ų�������ΪQ����t0ʱ�̣�����ƽ����ϵ�з�����ķ�֮һ�Ļ�����壬��ƽ����ϵ��c(A)Ϊ0.6mol��L��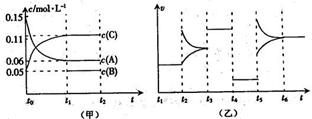
 A����Ӧ�ķ���ʽΪ3A(g)+B(g) 2C(g)
A����Ӧ�ķ���ʽΪ3A(g)+B(g) 2C(g)  4NO2(g)+O2(g) ��H>0
4NO2(g)+O2(g) ��H>0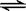 CO2(g)ʮH2 (g) ��H<0 �� CO��H2OŨ�ȱ仯����ͼ��
CO2(g)ʮH2 (g) ��H<0 �� CO��H2OŨ�ȱ仯����ͼ��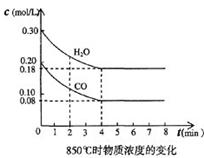
 2C��g������H��0������
2C��g������H��0������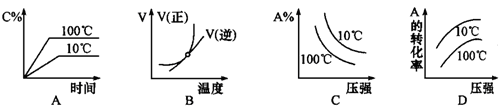
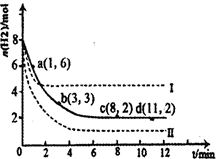
 CH3OH(g)��H2O(g)��H����49��0kJ��mol��1��ij��ѧʵ�齫6molCO2��8molH2����2L�ܱ������У����H2�����ʵ�����ʱ��仯����ͼ��ʾ��ʵ�ߣ���ͼ������a��1��6����������˼�ǣ���l minʱH2�����ʵ�����6mol��
CH3OH(g)��H2O(g)��H����49��0kJ��mol��1��ij��ѧʵ�齫6molCO2��8molH2����2L�ܱ������У����H2�����ʵ�����ʱ��仯����ͼ��ʾ��ʵ�ߣ���ͼ������a��1��6����������˼�ǣ���l minʱH2�����ʵ�����6mol��