题目内容
下列说法或表示方法正确的是
A.等物质的量的硫蒸气和固体硫分别完全燃烧,后者放出热量多
B.由C(石墨)= C(金刚石) △H=+1.90 kJ/mol可知,金刚石比石墨稳定
C.在101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:
2H2(g)+O2(g)=2H2O(l) △H=-285.8kJ/mol
D.在稀溶液中,H+(aq)+ OH-(aq)=H2O(l) △H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热大于57.3kJ
【答案】
D
【解析】
试题分析:A、固体硫的总能量低于气态硫的总能量,所以等物质的量的硫蒸气和固体硫分别完全燃烧,前者放出热量多,A不正确;B、由C(石墨)= C(金刚石) △H=+1.90 kJ/mol可知,金刚石的总能量高于石墨的总能量。能量越低越稳定,所以石墨比金刚石稳定,B不正确;C、燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的能量,2g氢气的物质的量是1mol,所以在101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:H2(g)+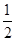 O2(g)=H2O(l) △H=-285.8kJ/mol,C不正确;D、中和热是在一定条件下,稀溶液中,强酸和强碱反应生成1mol水时所放出的热量。浓硫酸溶于水放热,因此在稀溶液中,H+(aq)+ OH-(aq)=H2O(l) △H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热大于57.3kJ,D正确,答案选D。
O2(g)=H2O(l) △H=-285.8kJ/mol,C不正确;D、中和热是在一定条件下,稀溶液中,强酸和强碱反应生成1mol水时所放出的热量。浓硫酸溶于水放热,因此在稀溶液中,H+(aq)+ OH-(aq)=H2O(l) △H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热大于57.3kJ,D正确,答案选D。
考点:考查反应热、中和热、燃烧热的有关判断和应用

练习册系列答案
相关题目
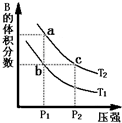 对于反应A(g)?2B(g)△H>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示.回答下列各题.
对于反应A(g)?2B(g)△H>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示.回答下列各题.

