题目内容
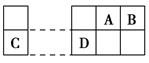
下列四种元素中,其单质氧化性最强的是( )。
| A.原子含有未成对电子最多的第2周期元素 |
| B.位于周期表第3周期ⅢA族的元素 |
| C.原子最外电子层排布式为2s22p6的元素 |
| D.原子最外电子层排布式为3s23p5的元素 |
D
解析

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
X、Y、Z、W是前20号元素,原子序数依次增大。X是原子半径最小的元素;Y元素原子的最外层电子数是电子层数的2倍;Z元素的-1价阴离子的核外电子排布与氖原子相同,W元素为金属,它的某种化合物可用于烟气脱硫。下列说法错误的是
| A.X、Y形成的化合物中可能含有双键 |
| B.X单质和Z单质在暗处能剧烈反应 |
C.W元素与Z元素形成的化合物用电子式表示形成过程为: |
| D.XZ的沸点在与Z同族的其它X的化合物中最高 |
元素周期律产生的根本原因就是随着元素原子序数的递增
| A.元素的相对原子质量逐渐增大 |
| B.核外电子排布呈周期性变化 |
| C.原子半径呈周期性变化 |
| D.元素主要化合价呈周期性变化 |
目前,医疗上使用放射性核素 治疗肿瘤,该核素原子核内的中子数与电子数之差是
治疗肿瘤,该核素原子核内的中子数与电子数之差是
| A.19 | B.53 | C.72 | D.125 |
不能说明X的电负性比Y的电负性大的是( )。
| A.与H2化合时X单质比Y单质容易 |
| B.X的最高价氧化物的水化物的酸性比Y的最高价氧化物的水化物的酸性强 |
| C.X原子的最外层电子数比Y原子最外层电子数多 |
| D.X单质可以把Y从其氢化物中置换出来 |
关于同一种元素的原子或离子,下列叙述正确的是( )。
| A.原子半径比阴离子半径小 |
| B.原子半径比阴离子半径大 |
| C.原子半径比阳离子半径小 |
| D.带正电荷多的阳离子比带正电荷少的阳离子半径大 |
各电子层排布电子的总数遵循以下规则:①每层最多容纳2n2个电子;②原子最外层电子数≤8;③原子次外层电子数≤18。决定这3条规律的电子排布规则是( )。
| A.能量最低原则 |
| B.泡利不相容原理 |
| C.洪特规则 |
| D.能量最低原则和泡利不相容原理 |
某粒子结构示意图为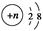 ,若该粒子为离子,则它所带的电荷数可能为( )。
,若该粒子为离子,则它所带的电荷数可能为( )。
①8-n ②n-8 ③10-n ④n-10
| A.①② | B.①③ | C.③④ | D.②④ |