题目内容
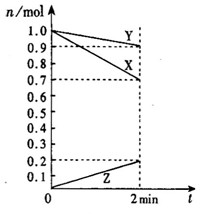
(10分)(1)(4分)某温度时,在2 L容器中,X、Y、Z三种物质的物质的量随时间变化曲线如图所示。由图中数据分析,该反应的化学方程式为:____________________________。反应开始至2 min,Z的平均反应速率为 __________。
(2)(6分)取a mol A和b mol B置于V L容器中,发生可逆反应:aA(g)+bB(g)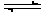 cC(g)+dD(g),1 min后,测得容器内A的浓度为x mol·L-1,这时B的浓度为: ;C的浓度为: 。在这段时间内反应速率若以物质A的浓度变化来表示,应为__________。
cC(g)+dD(g),1 min后,测得容器内A的浓度为x mol·L-1,这时B的浓度为: ;C的浓度为: 。在这段时间内反应速率若以物质A的浓度变化来表示,应为__________。

(2)(6分)取a mol A和b mol B置于V L容器中,发生可逆反应:aA(g)+bB(g)
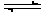 cC(g)+dD(g),1 min后,测得容器内A的浓度为x mol·L-1,这时B的浓度为: ;C的浓度为: 。在这段时间内反应速率若以物质A的浓度变化来表示,应为__________。
cC(g)+dD(g),1 min后,测得容器内A的浓度为x mol·L-1,这时B的浓度为: ;C的浓度为: 。在这段时间内反应速率若以物质A的浓度变化来表示,应为__________。(10分)(1)3X + Y 2Z;0.05 mol/L·min
2Z;0.05 mol/L·min
(2)bx/a;c/V-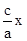 ;
;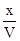 mol/L·min
mol/L·min
 2Z;0.05 mol/L·min
2Z;0.05 mol/L·min(2)bx/a;c/V-
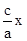 ;
;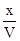 mol/L·min
mol/L·min(1)从图象上可以看出:X、Y减小而Z增加,变化的物质的量分别是1∶3∶2,所以反应为X+3Y 2Z;2 min末时Z的物质的量为0.2 mol,体积为2 L,所以反应速率为0.05 mol·(L·min)-1。
2Z;2 min末时Z的物质的量为0.2 mol,体积为2 L,所以反应速率为0.05 mol·(L·min)-1。
(3)aA(g)+bB(g)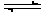 cC(g)+dD(g)
cC(g)+dD(g)
初c:a/V b/V 0 0
△c: a/V —x (a/V —x)b/a (a/V —x)c/a
1 min: V bx/a (a/V —x)c/a
 2Z;2 min末时Z的物质的量为0.2 mol,体积为2 L,所以反应速率为0.05 mol·(L·min)-1。
2Z;2 min末时Z的物质的量为0.2 mol,体积为2 L,所以反应速率为0.05 mol·(L·min)-1。(3)aA(g)+bB(g)
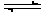 cC(g)+dD(g)
cC(g)+dD(g)初c:a/V b/V 0 0
△c: a/V —x (a/V —x)b/a (a/V —x)c/a
1 min: V bx/a (a/V —x)c/a

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
 2NH3(g) ΔH=-92.2 kJ· mol-1。平衡时,容器内气体压强为起始时的80%。
2NH3(g) ΔH=-92.2 kJ· mol-1。平衡时,容器内气体压强为起始时的80%。
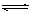 2C(气)+2D(固)达到平衡的标志的是( )
2C(气)+2D(固)达到平衡的标志的是( ) 2Z(g)已达到平衡的是
2Z(g)已达到平衡的是

 2Z,其平衡常数为1600
2Z,其平衡常数为1600 Q(g)达到平衡时,下列说法正确的是( )
Q(g)达到平衡时,下列说法正确的是( ) cC(g)+dD(g)改变条件达到平衡后D的浓度随条件改变的关系如下图,试判断此反应的系数关系和△H正负 ( )
cC(g)+dD(g)改变条件达到平衡后D的浓度随条件改变的关系如下图,试判断此反应的系数关系和△H正负 ( )