题目内容
(12分)A、B、C、D、E、F、G七种短周期主族元素的原子序数依次增大,D、G同主族,A与B、C、D能形成电子数相同的二种常见分子,E、F的原子序数之和是D的原子序数的3倍,D、E、F的简单离子具有相同电子层结构。
(1)三种元素的名称。B ,D ,F 。
(2)A与 D、A与G均可形成18e—的化合物。两种化合物在水溶液中反应的化学方程式为:
D、A与G均可形成18e—的化合物。两种化合物在水溶液中反应的化学方程式为:
(3) A、D、E三种元素中的两种或三种形成的物质中,含有非极性键的离子化合物的电子式为: ;只含离子键的化合物的电子式为: 。
(4)E离子的半径 (填“大于” “小于”或“等于”)F离子的半径;E 和F元素最高价氧化物对应的水化物之间反应的离子方程式为: 。
(5)写出由上述各种元素形成的粒子中与BC—电子数相等的三种分子的化学式 、 。
(1)三种元素的名称。B ,D ,F 。
(2)A与
 D、A与G均可形成18e—的化合物。两种化合物在水溶液中反应的化学方程式为:
D、A与G均可形成18e—的化合物。两种化合物在水溶液中反应的化学方程式为: (3) A、D、E三种元素中的两种或三种形成的物质中,含有非极性键的离子化合物的电子式为: ;只含离子键的化合物的电子式为: 。
(4)E离子的半径 (填“大于” “小于”或“等于”)F离子的半径;E 和F元素最高价氧化物对应的水化物之间反应的离子方程式为: 。
(5)写出由上述各种元素形成的粒子中与BC—电子数相等的三种分子的化学式 、 。
(12分)
(1)B 碳 ,D 氧 ,F 铝 。(各1分)
(2)H2O2+H2S=S↓+2H2O (2分)
(3)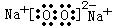 ;
; 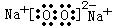 。(各1分)
。(各1分)
(4) 大于(1分) Al(OH)3+OH-=AlO2-+2H2O 。 (2分)
(6) N2 、 CO 。(各1分)
(1)B 碳 ,D 氧 ,F 铝 。(各1分)
(2)H2O2+H2S=S↓+2H2O (2分)
(3)
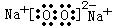 ;
; 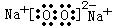 。(各1分)
。(各1分)(4) 大于(1分) Al(OH)3+OH-=AlO2-+2H2O 。 (2分)
(6) N2 、 CO 。(各1分)
略

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
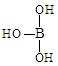 ,但硼酸溶于水后,1个硼酸分子与水作用,只能产生1个H+,请写出硼酸溶于水后溶液显酸性的离子方程式:
,但硼酸溶于水后,1个硼酸分子与水作用,只能产生1个H+,请写出硼酸溶于水后溶液显酸性的离子方程式: