题目内容
5.下列关于物质性质的叙述中,正确的是( )| A. | Cl2是一种活泼的非金属单质,在一定条件下能够和所有的金属反应 | |
| B. | N2是大气中的主要成分之一,雷雨时,可直接转化为NO2 | |
| C. | 硫是一种淡黄色的难溶于水的晶体,既有氧化性又有还原性 | |
| D. | 硅的用途广泛,常被用于制造石英表中的压电材料和光导纤维 |
分析 A、Cl2是一种活泼的非金属单质,与大多数金属发生反应;
B、空气中的氮气只有在雷雨放电条件下转化为NO,不能直接生成NO2;
C、硫单质是一种难溶于水的晶体,化合价处于中间价态分析;
D、制造石英表中的压电材料和光导纤维的材料是二氧化硅.
解答 解:A、氯气与大多数金属发生反应,与金、铂等不发生反应,故A错误;
B、N2是大气中的主要成分之一,雷雨时,氮气和氧气放电反应生成一氧化氮,不可直接转化为NO2,故B错误;
C、硫单质是一种难溶于水的晶体,化合价处于中间价态既有氧化性又有还原性,故C正确;
D、光导纤维和石英表中的压电材料的主要成分为二氧化硅,即二氧化硅常被用来制造光导纤维和石英表中的压电材料,故D错误;
故选C.
点评 本题考查了物质性质的分析,主要是氯气、氮气、硅、二氧化硅的性质分析应用,掌握基础是关键,题目较简单.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
15.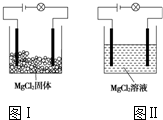 某化学兴趣小组进行化学实验,按照图Ⅰ连接好线路发现灯泡不亮,按照图Ⅱ连接好线路发现灯泡亮,由此得出的结论正确的是( )
某化学兴趣小组进行化学实验,按照图Ⅰ连接好线路发现灯泡不亮,按照图Ⅱ连接好线路发现灯泡亮,由此得出的结论正确的是( )
 某化学兴趣小组进行化学实验,按照图Ⅰ连接好线路发现灯泡不亮,按照图Ⅱ连接好线路发现灯泡亮,由此得出的结论正确的是( )
某化学兴趣小组进行化学实验,按照图Ⅰ连接好线路发现灯泡不亮,按照图Ⅱ连接好线路发现灯泡亮,由此得出的结论正确的是( )| A. | MgCl2是非电解 | |
| B. | MgCl2溶液是电解质 | |
| C. | MgCl2在水溶液中电离出了可以自由移动的离子 | |
| D. | MgCl2只有在溶液中才能导电 |
16.化学与环境密切相关,下列有关说法正确的是( )
| A. | CO2属于大气污染物 | |
| B. | 酸雨是pH小于7的雨水 | |
| C. | 大气中CO2含量的增加会导致温室效应加剧 | |
| D. | CO2、NO2或SO2都会导致酸雨的形成 |
13.HA为酸性略强于醋酸的一元弱酸,则下列叙述正确的是( )
| A. | 0.1 mol•L-1 HA溶液与0.1 mol•L-1 NaOH溶液混合至溶液呈中性:c(Na+)>c(A-) | |
| B. | 0.1 mol•L-1 HA溶液中:c(H+)=c(OH-)+c(A-) | |
| C. | 0.1 mol•L-1 NaA溶液中:c(Na+)>c(OH-)>c(A-)>c(H+) | |
| D. | 0.1 mol•L-1 HA溶液中加入少量NaA固体,HA的电离常数减小 |
20.下列各组表述中,两个微粒属于同种元素原子的是( )
| A. | M层全充满而N层为4s2的原子和核外电子排布为1s22s22p63s23p63d64s2 的原子 | |
| B. | 2p能级有一个未成对电子的基态原子和原子的价电子排布为2s22p5 | |
| C. | 3p能级有一个空轨道的基态原子和核外电子的排布为1s22s22p63s23p2 | |
| D. | 最外层电子数是核外电子总数的1/5的原子和价电子排布为4s24p1的原子 |
17.据报道,某些花岗岩会产生放射性元素氡(${\;}_{86}^{222}$Rn),下列说法中不正确的是( )
| A. | 该原子的质量数为222 | B. | Rn是86号元素 | ||
| C. | 一个222 86Rn原子中有136个中子 | D. | 一个222 86Rn原子中有136个电子 |
14.化学实验有助于理解化学知识,形成化学观念.下列实验操作正确的是( )
| A. |  称量药品 | B. | 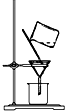 过滤 | C. | 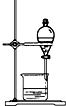 分离乙醇和水 | D. | 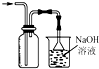 收集氯气 |
15.现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)A基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤 形,A与氢元素形成化合物AH5除了配位键外还有离子键和极性键.
(2)某同学根据上述信息,所画的C电子排布图如图违背了泡利 原理.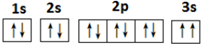
(3)DE3 中心原子的杂化方式为sp3,用价层电子对互斥理论推测其分子空间构型为三角锥形.检验F元素的方法是焰色反应.
(4)A2与B22+互为等电子体,B22+的电子式可表示为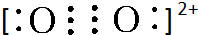 ;1mol B22+中含有的π键数目为2NA.
;1mol B22+中含有的π键数目为2NA.
(5)下列电子云图象均为成键后电子云图象,其中可表示一个E原子与一个E原子的是E,表示一个氢原子与一个E原子的是D.

| A.元素原子的核外p电子总数比s电子总数少1 |
| B.元素价电子排布式为nsnnp2n |
| C.元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期 |
| D.原子核外所有p轨道全满或半满 |
| E.元素的主族序数与周期数的差为4 |
| F.是前四周期中电负性最小的元素 |
(2)某同学根据上述信息,所画的C电子排布图如图违背了泡利 原理.

(3)DE3 中心原子的杂化方式为sp3,用价层电子对互斥理论推测其分子空间构型为三角锥形.检验F元素的方法是焰色反应.
(4)A2与B22+互为等电子体,B22+的电子式可表示为
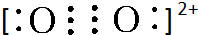 ;1mol B22+中含有的π键数目为2NA.
;1mol B22+中含有的π键数目为2NA.(5)下列电子云图象均为成键后电子云图象,其中可表示一个E原子与一个E原子的是E,表示一个氢原子与一个E原子的是D.
