题目内容
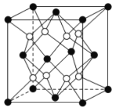
【题目】有关晶体的结构如图所示,下列说法中不正确的是( )

A.在NaCl晶体中,距Na+最近的Cl-有6个
B.在CaF2晶体中,每个晶胞平均占有4个Ca2+
C.在金刚石晶体中,最小的环上有6个C原子
D.该气态团簇分子的分子式为EF或FE
【答案】D
【解析】
A.以顶点Na+研究,与之最近的Cl-处于晶胞棱心且关于Na+对称,即距Na+最近的Cl-有6个,故A正确;
B.在CaF2晶体中,Ca2+位于晶胞顶点和面心,数目为8×![]() +6×
+6×![]() =4,即每个晶胞平均占有4个Ca2+,故B正确;
=4,即每个晶胞平均占有4个Ca2+,故B正确;
C.金刚石晶体中,由共价键形成的最小碳环上有6个碳原子,每个碳原子形成四个共价键,从而形成空间网状结构,由金刚石的晶胞结构图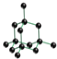 ,也可以看出最小的环上有6个碳原子,故C正确;
,也可以看出最小的环上有6个碳原子,故C正确;
D.该气态团簇分子中含有4个E、4个F原子,分子式应为E4F4或F4E4,故D错误;
答案为D。

 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案【题目】重铬酸钾别名为红矾钾,室温下为橙红色晶体,溶于水,不溶于乙醇。它被国际癌症研究机构划归为第一类致癌物质,而且是强氧化剂,在实验室和工业中都有很广泛的应用。实验小组研究酸性条件下K2Cr2O7溶液和H2O2溶液的反应。相关资料如下:
序号 | 资料 |
① | Cr2(SO4)3溶液呈绿色 |
② | 酸性条件下,K2Cr2O7溶液和H2O2溶液反应生成CrO5,CrO5进一步反应生成Cr3+和O2 |
③ | CrO5可溶于水,易溶于乙醚得到蓝色溶液 |
④ | 乙醚是一种无色不溶于水,密度比水小的有机溶剂,化学性质稳定 |
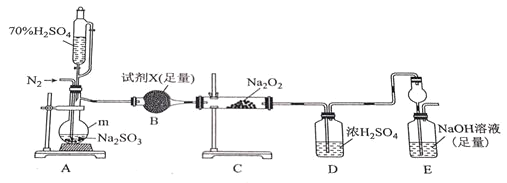
甲同学采用如图装置进行实验,探究了酸性条件下K2Cr2O7溶液和H2O2溶液的反应产物,实验步骤、操作等内容如下:
实验步骤 | 实验操作 | 实验现象 |
Ⅰ | 组装仪器 | —— |
Ⅱ | ? | —— |
Ⅲ | 向盛有H2O2溶液的仪器X中加入一定量的K2Cr2O7溶液和硫酸 | 溶液立即变为紫红色,此时pH=1,观察到溶液中持续产生气泡,最终溶液变为绿色 |
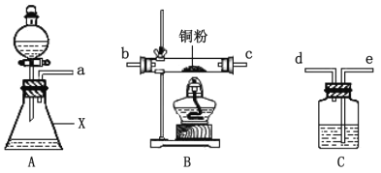
回答下列问题:
(1)用以上装置证明实验中产生的气体有氧气,装置的连接顺序是a→__→__→__→__。
(2)图中仪器X的名称是___。
(3)实验步骤Ⅱ是___。
(4)实验中紫红色溶液含有CrO5。
①验证紫红色溶液中含有CrO5的操作及现象是___。
②已知CrO5的结构式为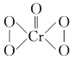 ,生CrO5的反应,不是氧化还原反应,则该反应的离子方程式为___。
,生CrO5的反应,不是氧化还原反应,则该反应的离子方程式为___。
(5)对上述实验中产生氧气、溶液变为绿色的原因,做出的假设①是CrO5在酸性溶液中不稳定,自身氧化还原生成Cr3+和O2。你还能做出的假设②是___。
(6)设计实验,选择合适的试剂,验证(5)中的假设①,你的设计是___。
【题目】下图是元素周期表的一部分:
C | N | O | F | ||
Si | P | S | Cl | ||
Ge | As | Se | Br | ||
Sn | Sb | Te | I | ||
Pb | Bi | Po | At | ||
![]() 阴影部分元素的外围电子排布式的通式为____。Sb的元素名称为____。基态P原子中,电子占据的最高能级符号为____,该能层具有的原子轨道数为____。
阴影部分元素的外围电子排布式的通式为____。Sb的元素名称为____。基态P原子中,电子占据的最高能级符号为____,该能层具有的原子轨道数为____。
![]() 氮族元素氢化物
氮族元素氢化物![]() 、
、![]() 、
、![]() 的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物
的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物![]() 性质可能有____。
性质可能有____。
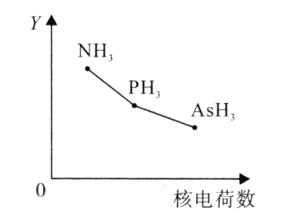
A.稳定性
B.沸点
C.![]() 键能
键能
D.分子间作用力
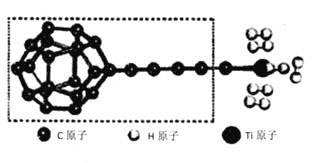
![]() 某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有____种。
某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有____种。
![]() 和
和![]() 、
、![]() 及
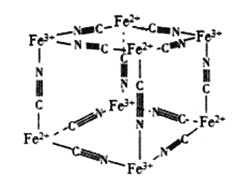
及![]() 能形成一种蓝色配位化合物普鲁士蓝。如图是该物质的结构单元
能形成一种蓝色配位化合物普鲁士蓝。如图是该物质的结构单元![]() 未标出
未标出![]() ,该图是普鲁士蓝的晶胞吗?____
,该图是普鲁士蓝的晶胞吗?____![]() 填“是”或“不是”
填“是”或“不是”![]() ,平均每个结构单元中含有____个
,平均每个结构单元中含有____个![]() 。
。
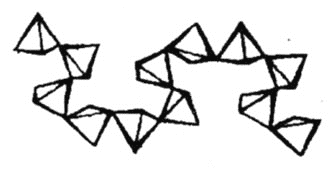
![]() 磷酸盐与硅酸盐之间具有几何形态的相似性。如多磷酸盐与多硅酸盐一样,也是通过四面体单元通过共用顶角氧离子形成岛状、链状、层状、骨架网状等结构型式。不同的是多硅酸盐中是
磷酸盐与硅酸盐之间具有几何形态的相似性。如多磷酸盐与多硅酸盐一样,也是通过四面体单元通过共用顶角氧离子形成岛状、链状、层状、骨架网状等结构型式。不同的是多硅酸盐中是![]() 四面体,多磷酸盐中是
四面体,多磷酸盐中是![]() 四面体。下图为一种无限长单链结构的多磷酸根,该多磷酸根的化学式为____。
四面体。下图为一种无限长单链结构的多磷酸根,该多磷酸根的化学式为____。