题目内容
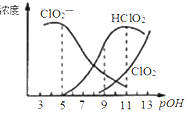
【题目】亚氯酸钠(NaClO2)用于漂白织物、纤维、纸浆,具有对纤维损伤小的特点。其在溶液中可生成ClO2、HClO2、ClO2-、Cl- 等,其中HClO2和ClO2都具有漂白作用。已知POH =-lgc(OH-),经测定25℃时各组分含量随POH变化情况如图所示(Cl-没有画出),此温度下,下列分析错误的是( )
A.亚氯酸钠在碱性条件下较稳定
B.PH=7时,溶液中含氯微粒的浓度大小:c(ClO2—)﹥c(HClO2)﹥c (ClO2)
C.HClO2的电离平衡常数的数值Ka=10-6
D.同浓度的HClO2溶液和NaClO2溶液等体积混合,则混合溶液中有2c(HClO2)+c(H+)=2c(ClO2—) + c(OH-)
【答案】D
【解析】
试题分析:A、由图可以得出:碱性条件下ClO2-浓度高,即在碱性条件下亚氯酸钠较稳定,故A正确;B、根据图知,pH=7时,存在c(HClO2)<c( ClO2-),则微粒浓度大小顺序是c( ClO2-)>c(HClO2)>c( ClO2)>c( Cl-),故B正确;C、HClO2的电离平衡常数K=![]() ,观察图象可以看出,当pOH=8时,pH=6,c(ClO2-)=c(HClO2),因此HClO2的电离平衡常数的数值Ka=10-6,故C正确;D、依据电中性原则得出:c(H+)+c(Na+)=c(ClO2-)+c(OH-) ①,依据物料守恒得出:2c(Na+)=c(ClO2-)+c(HClO2) ②,联立①②消去钠离子:c(HClO2)+2c(H+)=c(ClO2-)+2c(OH-),故D错误;故选D。
,观察图象可以看出,当pOH=8时,pH=6,c(ClO2-)=c(HClO2),因此HClO2的电离平衡常数的数值Ka=10-6,故C正确;D、依据电中性原则得出:c(H+)+c(Na+)=c(ClO2-)+c(OH-) ①,依据物料守恒得出:2c(Na+)=c(ClO2-)+c(HClO2) ②,联立①②消去钠离子:c(HClO2)+2c(H+)=c(ClO2-)+2c(OH-),故D错误;故选D。

练习册系列答案
相关题目