题目内容
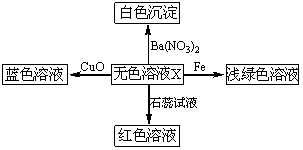
A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如下图所示:

请回答下列问题:
(1)若A为金属单质,B为非金属氧化物,则该反应的化学方程式为 ;请写出质量数为26的A的一种核素符号 。
(2)若A为金属单质,B为黑色磁性晶体,则该反应的化学方程式为 ;请写出A与氢氧化钠溶液反应的离子方程式 ;

请回答下列问题:
(1)若A为金属单质,B为非金属氧化物,则该反应的化学方程式为 ;请写出质量数为26的A的一种核素符号 。
(2)若A为金属单质,B为黑色磁性晶体,则该反应的化学方程式为 ;请写出A与氢氧化钠溶液反应的离子方程式 ;
(1)2Mg+CO2 2MgO+C
2MgO+C 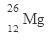
(2)8Al+3Fe3O4 9Fe+4Al2O3 2Al+2OH-+2H2O=2AlO2-+3H2↑
9Fe+4Al2O3 2Al+2OH-+2H2O=2AlO2-+3H2↑
 2MgO+C
2MgO+C 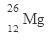
(2)8Al+3Fe3O4
 9Fe+4Al2O3 2Al+2OH-+2H2O=2AlO2-+3H2↑
9Fe+4Al2O3 2Al+2OH-+2H2O=2AlO2-+3H2↑试题分析:(1)若A为金属单质,B为非金属氧化物,符合框图要求的可以是Fe与H2O、Mg与CO2等。若与后面的要求—写出质量数为26的A的一种核素符号则前者就不符合要求了。故反应方程式为2Mg+CO2
 2MgO+C。A的质量数为26的一种核素符号
2MgO+C。A的质量数为26的一种核素符号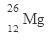 。(2)黑色磁性晶体为Fe3O4,能与金属氧化物发生置换反应的金属只有Al的铝热反应。反应的方程式为8Al+3Fe3O4
。(2)黑色磁性晶体为Fe3O4,能与金属氧化物发生置换反应的金属只有Al的铝热反应。反应的方程式为8Al+3Fe3O4 9Fe+4Al2O3。Al与氢氧化钠溶液反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑。
9Fe+4Al2O3。Al与氢氧化钠溶液反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑。
练习册系列答案
 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目

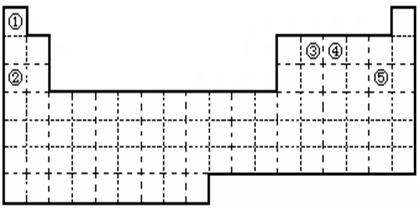
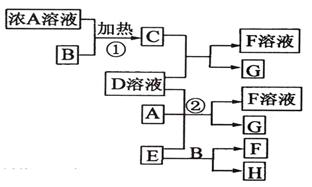

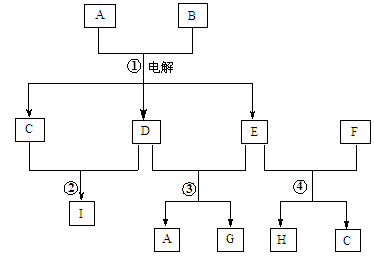
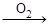 乙
乙 丁,其中丁为强酸,则甲不可能为
丁,其中丁为强酸,则甲不可能为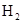 比l mol b从酸中置换
比l mol b从酸中置换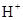 生成的
生成的