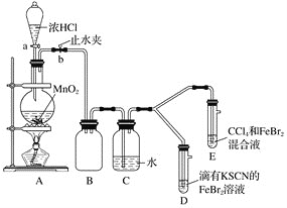
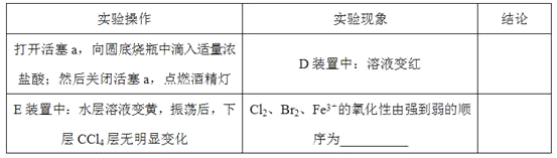
题目内容
【题目】①C(s)+![]() O2(g)=CO(g) ΔH=-110.5 kJ/mol,②C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol,则CO的燃烧热为_______,其热化学方程式为________。
O2(g)=CO(g) ΔH=-110.5 kJ/mol,②C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol,则CO的燃烧热为_______,其热化学方程式为________。
【答案】283.0kJ/mol CO(g)+ ![]() O2(g)=CO2(g)△H=-283.0 kJ/mol
O2(g)=CO2(g)△H=-283.0 kJ/mol
【解析】
由盖斯定律可知②—①可得表示CO燃烧热的热化学方程式,CO(g)+ ![]() O2(g)=CO2(g),则△H=△H2—△H1=(-393.5 kJ/mol)—(-110.5kJ/mol)=-283.0kJ/mol,热化学方程式为CO(g)+
O2(g)=CO2(g),则△H=△H2—△H1=(-393.5 kJ/mol)—(-110.5kJ/mol)=-283.0kJ/mol,热化学方程式为CO(g)+ ![]() O2(g)=CO2(g)△H=-283.0 kJ/mol,故答案为:283.0kJ/mol ;CO(g)+
O2(g)=CO2(g)△H=-283.0 kJ/mol,故答案为:283.0kJ/mol ;CO(g)+ ![]() O2(g)=CO2(g)△H=-283.0 kJ/mol。
O2(g)=CO2(g)△H=-283.0 kJ/mol。

 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案【题目】[化学一选修3:物质结构与性质
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Ti3+的未成对电子数有__________个。
②LiBH4由Li+和BH4-构成,BH4-的空间构型是__________,B原子的杂化轨道类型是_____。
③某储氢材料是第三周期金属元素M的氢化物,M的部分电离能如下表所示:
I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
738 | 1451 | 7733 | 10540 | 13630 |
M是_______(填元素符号),判断理由为_______________。
(2)铜晶体中铜原子的堆积方式如图所示,铜晶体中原子的堆积模型属于____________。

(3)A原子的价电子排布式为3s23p5,铜与A 形成化合物的晶胞如图所示(黑点代表铜原子)。
①该晶体的化学式为______________。
②该化合物难溶于水但易溶于氨水,其原因是_____________ ,此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为____________。
③己知该晶体的密度为ρg·cm-3,阿伏伽德罗常数为NA,己知该晶体中Cu原子和A原子之间的最短距离为体对角线的1/4,则该晶体中Cu原子和A原子之间的最短距离为________pm。
【题目】金属冶炼、电镀、电路板生产等过程会产生大量的 Cu2+,Cu2+是一种重金属离子,严重影响水生动植物的生长发育,对人体健康也有很大危害,必须经过处理达标后方可排放。某电路板生产企业的水质情况及国家允许排放的污水标准如下表:
项目 | 废水水质 | 排放标准 |
pH | 1.0 | 6~9 |
Cu2+(mg/L) | 1470 | ≤0.5 |
氨氮(mg/L) | 2632 | ≤15 |
Ⅰ.为研究上述废水中 Cu2+的处理方法并实现 Cu 的资源化回收,有研究者进行了如下实验: 向一定体积的废水中加入一定量废铁屑和焦炭粉,置于搅拌器上搅拌 90min、静置,经分析测得上清液中铜含量约为 72mg/L;滤出上清液,向滤液中加入一定量 FeS 固体,充分搅拌后静置,经分析测得其中铜含量已经达标。
(1)在 pH=1.0 的废水中,氨氮的主要存在形式是_____(用化学式表示)。
(2)①加入废铁屑后,废水中的铜含量明显减少,反应的离子方程式是_____
②加入焦炭可以加快反应速率,原因是_________________________________
(3)结合化学用语解释加入 FeS 固体使废水达标的原因_________________________。
(4)在处理废水过程中使用的铁粉会因表面布满一层铜膜而失效,因此要对失效的铁粉进行活化处理,同时回收铜。处理方法为:用一定浓度的氨水浸泡包覆铜膜的铁粉,露置在空气中一段时间后,可以将表面的 Cu 转化为[Cu(NH3)4]2+与铁粉分离。
请写出 Cu 转化为 [Cu(NH3)4]2+的离子方程式:_____。
Ⅱ为研究废水处理的最佳 pH,取五份等量的 I 中上清液, 分别用 30%的 NaOH 溶液调节 pH 值至 8.5、9、9.5、10、11,静置后,分析上层清液中铜元素的含量。实验结果如图所示。查阅资料可知:Cu(OH)2 + 4NH3![]() [Cu(NH3)4]2+ + 2OH-。
[Cu(NH3)4]2+ + 2OH-。
(5)根据实验结果,你认为最佳的 pH 约为_____________________________。结合资料解释实验结果呈图中 b~d 段曲线所示的原因:_________________________。