题目内容
3.与H2O具有相同电子数的是( )| A. | F | B. | O2 | C. | CH4 | D. | C2H6 |
分析 H2O分子具有10个电子,根据常见的10电子微粒来解答.
解答 解:原子或分子中电子数等于质子数,H2O分子具有10个电子,与H2O分子具有相同电子数的分子有Ne、HF、NH3、CH4等,故选C.
点评 本题考查了常见的10电子微粒,根据原子或分子中电子数等于质子数判断,题目难度不大.

练习册系列答案
相关题目
14.下列物质中既含有共价键又含有离子键的是( )
| A. | KOH | B. | MgO | C. | H2SO4 | D. | CO2 |
11.${\;}_{27}^{69}$Co是放射性元素,它的核内中子数为( )
| A. | 60 | B. | 27 | C. | 33 | D. | 42 |
18.下列叙述不正确的是( )
| A. | 需要加热的反应一定是吸热反应 | |
| B. | 化学反应就是旧化学键断裂、新化学键形成的过程 | |
| C. | 化学反应一定伴随着能量的变化 | |
| D. | 化石燃料并非在任何情况下都能充分燃烧 |
8.(1)下表示元素周期表的一部分
①写出元素符号:fSi;hCl;
②c、d、e、b的原子半径由大到小的顺序是Na>Mg>Al>F;
③g、h的最高价氧化物的水化物中酸性强的是HClO4;
④a、f的氢化物中稳定性强的是SiH4.
⑤a元素和氢元素形成的化合物的电子式是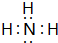 .
.
⑥c元素和b元素形成的化合物中含有的化学键类型是离子键.
(2)下表是元素周期表的一个片段,各元素均属于短周期元素
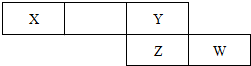
①若X的单质为空气的主要成分之一,则W的原子结构示意图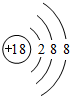 ;
;
②若Y能与钠形成反应生成淡黄色固体,则该淡黄色固体的化学式为Na2O2;含有的化学键类型有离子键、共价键.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | a | b | ||||||
| 3 | c | d | e | f | g | h | i |
②c、d、e、b的原子半径由大到小的顺序是Na>Mg>Al>F;
③g、h的最高价氧化物的水化物中酸性强的是HClO4;
④a、f的氢化物中稳定性强的是SiH4.
⑤a元素和氢元素形成的化合物的电子式是
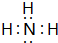 .
.⑥c元素和b元素形成的化合物中含有的化学键类型是离子键.
(2)下表是元素周期表的一个片段,各元素均属于短周期元素

①若X的单质为空气的主要成分之一,则W的原子结构示意图
 ;
;②若Y能与钠形成反应生成淡黄色固体,则该淡黄色固体的化学式为Na2O2;含有的化学键类型有离子键、共价键.
15.下列各组混合物中,不论两种物质以何种比例混合,只要总物质的量一定,完全燃烧后,消耗O2的质量不变的是( )
| A. | 乙炔和苯 | B. | 甲醛与乙醛 | C. | 甲烷和乙酸 | D. | 丙烯和丁烯 |
12.乙酸具有的官能团是( )
| A. | 碳碳双键 | B. | 羟基 | C. | 醛基 | D. | 羧基 |
13.下列叙述错误的是( )
| A. | 吸热反应的反应物总能量低于生成物总能量 | |
| B. | 绿色植物进行光合作用时,将光能转化为化学能“贮存”起来 | |
| C. | 电力属于一次能源 | |
| D. | 物质的化学能可以在不同条件下转为热能、电能、光能等为人类所利用 |

