题目内容
研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
(1)C、Si、N元素的电负性由大到小的顺序是 ,
C60和金刚石都是碳的同素异形体,二者相比,熔点高的是 ,原因是 。
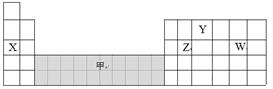
(2)A、B均为短周期金属元素,依据表中数据,写出B的基态原子的电子排布式: 。
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,d0或d10排布无颜色,d1~d9排布有颜色。如[Co(H2O)6]2+显粉红色。据此判断:[Mn(H2O)6]2+ (填“无”或“有”)颜色。
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。
①COCl2分子的结构式为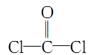 ,每个COCl2分子内含有 个σ键, 个π键,其中心原子采取 杂化轨道方式。
,每个COCl2分子内含有 个σ键, 个π键,其中心原子采取 杂化轨道方式。
②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g)。反应过程中,断裂的化学键只有配位键,则形成的化学键类型是 。
(1)C、Si、N元素的电负性由大到小的顺序是 ,
C60和金刚石都是碳的同素异形体,二者相比,熔点高的是 ,原因是 。
(2)A、B均为短周期金属元素,依据表中数据,写出B的基态原子的电子排布式: 。
| 电离能/(kJ·mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。
①COCl2分子的结构式为
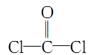 ,每个COCl2分子内含有 个σ键, 个π键,其中心原子采取 杂化轨道方式。
,每个COCl2分子内含有 个σ键, 个π键,其中心原子采取 杂化轨道方式。②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g)。反应过程中,断裂的化学键只有配位键,则形成的化学键类型是 。
(1)N>C>Si 金刚石 金刚石为原子晶体,C60为分子晶体
(2)1s22s22p63s2
(3)有
(4)①3 1 sp2 ②金属键
(2)1s22s22p63s2
(3)有
(4)①3 1 sp2 ②金属键
(1)非金属性越强,元素电负性越大,根据三种元素在元素周期表中的位置,可知它们的电负性关系是N>C>Si。C60是分子晶体,金刚石是原子晶体,金刚石的熔点较高。(2)从表中电离能数值来看,A、B的第三电离能出现突跃,可见它们是第ⅡA族元素,因A、B均为短周期元素,且B的第一、二电离能均比A的小,故B是镁。(3)Mn2+的3d轨道有5个电子,故[Mn(H2O)6]2+有颜色。(4)①单键是σ键,双键中有一个σ键和一个π键。因碳、氧形成双键,故碳原子采取的是sp2杂化。②Fe(CO)5的配位键是铁原子与CO形成的,分解产物CO的化学键并未改变,生成了铁单质,故形成的化学键是金属键。

练习册系列答案
相关题目