题目内容
【题目】Ⅰ.在![]() 密闭容器中放入
密闭容器中放入![]() ,在一定温度进行如下反应:
,在一定温度进行如下反应:![]()
容器内气体总压强(P)与起始压强![]() 的比值随反应时间(t)数据见下表:(提示,密闭容器中的压强比等于气体物质的量之比)
的比值随反应时间(t)数据见下表:(提示,密闭容器中的压强比等于气体物质的量之比)
时间 | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | |
| 1.00 | 1.50 | 1.80 | 2.20 | 2.30 | 2.38 | 2.40 | 2.40 |
回答下列问题
(1)下列能提高A的转化率的是_______
A.升高温度 B.体系中通入A气体
C.将D的浓度减小 D.通入稀有气体![]() ,使体系压强增大到原的5倍
,使体系压强增大到原的5倍
(2)该反应的平衡常数的表达式K_______,前2小时C的反应速率是_________![]() ;
;
(3)平衡时A的转化率___________,C的体积分数__________(均保留两位有效数字)
(4)相同条件下,若该反应从逆向开始,建立与上述相同的化学平衡,则D的物质的量取值范围![]() ______
______![]()
Ⅱ.已知乙酸是一种重要的化工原料,该反应所用的原理与工业合成乙酸的原理类似;常温下,将![]() 溶于水配成
溶于水配成![]() 溶液,向其中滴加等体积的
溶液,向其中滴加等体积的![]() 的盐酸使溶液呈中性(不考虑醋酸和盐酸的挥发),用含a和b的代数式表示醋酸的电离常数
的盐酸使溶液呈中性(不考虑醋酸和盐酸的挥发),用含a和b的代数式表示醋酸的电离常数![]() ___________
___________
【答案】A 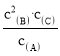 0.02
0.02 ![]()
![]() 0.03
0.03 ![]()
【解析】
Ⅰ. (1)提高反应物的转化率,使得化学平衡正向进行的因素均可以(但是不能加入物质本身);
(2)化学平衡常数![]() ,化学反应速率
,化学反应速率![]() 来计算;
来计算;
(3)根据三行式计算化学反应中物质的转化率以及物质的体积分数;
(4)若该反应从逆向开始,建立与上述相同的化学平衡,则Qc>K,根据极限转化思想来实现等效平衡;
Ⅱ. 根据电荷守恒结合平衡常数表达式计算。
Ⅰ. (1)A. 该反应正反应为吸热反应,升高温度,平衡正向移动,A的转化率增大,A正确;
B. 体系中通入A气体,A的转化率减小,B错误;
C. D为固体,将D的浓度减小,不会引起平衡的移动,A的转化率不变,C错误;
D. 通入稀有气体He,使体系压强增大到原来的5倍,但是各组分浓度不变,不会引起平衡的移动,A的转化率不变,D错误;故答案为:A;
(2)化学平衡常数 ,在1.0L密闭容器中放入0.10molA(g),设A的变化量为x,则根据三段式:
,在1.0L密闭容器中放入0.10molA(g),设A的变化量为x,则根据三段式:
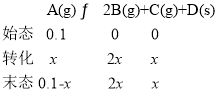
则![]() ,解得x=0.04mol,所以前2小时A的反应速率为:
,解得x=0.04mol,所以前2小时A的反应速率为: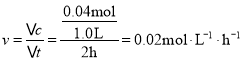 ,物质表示的反应速率之比等于系数之比,所以C表示的反应速率为:
,物质表示的反应速率之比等于系数之比,所以C表示的反应速率为:![]() ,故答案为:
,故答案为: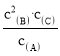 ;0.02;
;0.02;
(3)设:平衡时A的变化量是y,则根据三段式:
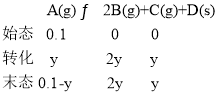
化学反应在20h时达到平衡,则![]() ,解得y=0.07mol,所以平衡时A的转化率为:
,解得y=0.07mol,所以平衡时A的转化率为:![]() ,C的体积分数为:
,C的体积分数为:![]() ,故答案为:
,故答案为:![]() ;
;![]() ;
;
(4)相同条件下,若该反应从逆向开始,建立与上述相同的化学平衡,则D的取值范围n(D)>0.03mol,故答案为:0.03;
Ⅱ. 盐酸和醋酸钠反应生成氯化钠和醋酸,溶液呈中性,所以醋酸钠剩余,c(H+)=c(OH-)=107mol/L,根据电荷守恒,c(Cl-)=0.5bmol/L,c(CH3COO-)+c(Cl-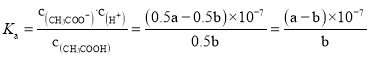 ,故答案为:
,故答案为:![]() 。
。

 阅读快车系列答案
阅读快车系列答案