��Ŀ����
����Ŀ����10�֣���ͼ��ʵ�������Ʊ��������֤�������ʵ�װ��ͼ��

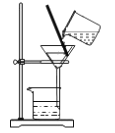
��1������a��������_________________________��
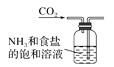
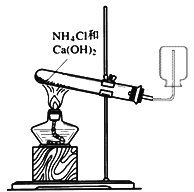
��2��������ͼװ���Ʊ������������������
��Բ����ƿ�ڷ�����Ӧ�����ӷ���ʽΪ________________________________________��
��װ��B����ҺΪ________________���ձ�E����Һ������Ϊ_______________________��
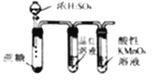
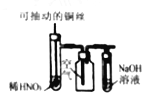
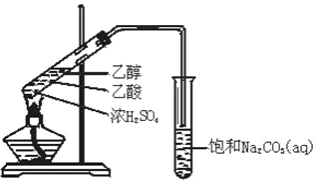
��3������ͼװ��֤��SO2����Ư���ԡ���ԭ�Լ����������к���CO2��
Բ����ƿ�ڼ���̼��a�м���Ũ���ᣬB��D�о�Ϊ����Ʒ����Һ��C��Ϊ�������Ը��������Һ��E��Ϊ����ʯ��ˮ��
��֤��SO2����Ư���Ե�װ����_______________��������______________________��
��֤��SO2���л�ԭ�Ե�������_____________________________________________��
��֤�����������к���CO2��������_________________________________________��
��Dװ�õ�������________________________________________��
���𰸡���10�֣���1����Һ©��
��2����4H++2Cl-+MnO2![]() 2H2O + Cl2��+Mn2+
2H2O + Cl2��+Mn2+
������ʳ��ˮ ����������ֹ��Ⱦ
��3����B Ʒ����ɫ��C�е�KMnO4��Һ��ɫ
��D��Ʒ�첻��ɫ��E��ʯ��ˮ�������������������Ƿ����
��������
������1��������a��ͼ�ο�֪a�Ƿ�Һ©����
��2����Բ����ƿ�ڷ����ķ�Ӧ��ʵ������ȡ�����ķ�Ӧ�����ӷ���ʽΪ4H++2Cl-+MnO2![]() 2H2O + Cl2��+Mn2+
2H2O + Cl2��+Mn2+
��װ��B��Ŀ���dz�ȥ�����е�HCl������B����ҺΪ����ʳ��ˮ���ձ�E��������β������������ʣ�����������ֹ��Ⱦ��
��3��B�е�Ʒ����Һ��֤���������Ư���ԣ�C����������֤��������Ļ�ԭ�ԣ�D�е�Ʒ��������֤Ʒ���Ƿ������E�е�ʯ��ˮ��֤������̼�Ĵ��ڡ��������������ʹƷ����Һ��ɫ������֤��SO2����Ư���Ե�װ����B��B�е�Ʒ����ɫ����֤����
������������л�ԭ�ԣ���ʹ���Ը��������Һ��ɫ������֤��SO2���л�ԭ�Ե�������C�е�KMnO4��Һ��ɫ
������������E֮ǰӦ��ȥ������֤�����������к���CO2��������D��Ʒ�첻��ɫ��E��ʯ��ˮ����ǣ�
��Dװ�õ������Ǽ�����������Ƿ������

����Ŀ�����Ļ����������������й㷺���ڡ�
(1)���Ȱ���NH2Cl���ĵ���ʽΪ________����ͨ����ӦNH3(g)��Cl2(g)=NH2Cl(g)��HCl(g)�Ʊ��Ȱ�����֪���ֻ�ѧ���ļ������ұ���ʾ���ٶ���ͬ������ͬ�ֻ�ѧ���ļ���һ��������������Ӧ�Ħ�H=_________��
��ѧ�� | ����/(kJ��mol-1) |
N-H | 391.3 |
Cl-Cl | 243.0 |
N-Cl | 191.2 |
H-Cl | 431.8 |
��NH2Cl��ˮ��Ӧ����ǿ�����Ե����ʣ�������Ч�������������÷�Ӧ�Ļ�ѧ����ʽΪ________��
(2)�ý�̿��ԭNO�ķ�ӦΪ��2NO(g)+C(s)![]() N2(g)+CO2(g)�����ݻ���Ϊ1L�ļס��ҡ����������ݺ��£���Ӧ�¶ȷֱ�Ϊ400�桢400�桢T�棩�����зֱ���������Ľ�̿��һ������NO����ø�������n(NO)�淴Ӧʱ��t�ı仯������±���ʾ��
N2(g)+CO2(g)�����ݻ���Ϊ1L�ļס��ҡ����������ݺ��£���Ӧ�¶ȷֱ�Ϊ400�桢400�桢T�棩�����зֱ���������Ľ�̿��һ������NO����ø�������n(NO)�淴Ӧʱ��t�ı仯������±���ʾ��
t/min | 0 | 40 | 80 | 120 | 160 |
n(NO)����������/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
n(NO)����������/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
n(NO)����������/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
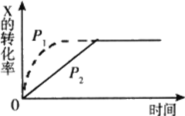
�ٸ÷�ӦΪ____________������ȡ������ȡ�����Ӧ��
����������200min�ﵽƽ��״̬����0��200min����NO��Ũ�ȱ仯��ʾ��ƽ����Ӧ����v(NO)=_________��
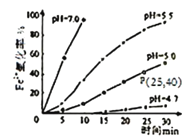
(3)�ý�̿��ԭNO2�ķ�ӦΪ��2NO2(g)+2C(s) ![]() N2(g)+2CO2(g)���ں��������£�1molNO2������C�����÷�Ӧ�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��
N2(g)+2CO2(g)���ں��������£�1molNO2������C�����÷�Ӧ�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��

��A��B�����Ũ��ƽ�ⳣ����ϵ��Kc(A)_____Kc(B)�������������=������
��A��B��C������NO2��ת������ߵ���______���A����B����C�����㡣
�ۼ���C��ʱ�÷�Ӧ��ѹǿƽ�ⳣ��Kp(C)=______��Kp����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ�����ʵ�����������