题目内容
某待测液可能有Fe2+、Fe3+、Ag+、Ba2+、Al3+、Ca2+、NH4+等离子,进行了下述实验(所加酸、碱、NH3水、Br2水都是过量的)。

根据实验结果:
(1)判定待测液中有无Ba2+、Ca2+离子,并写出理由。答_________。
(2)写出沉淀D的分子式:_________。
(3)写出从溶液D生成沉淀E的离子反应方程式:_________。

根据实验结果:
(1)判定待测液中有无Ba2+、Ca2+离子,并写出理由。答_________。
(2)写出沉淀D的分子式:_________。
(3)写出从溶液D生成沉淀E的离子反应方程式:_________。
(1)含有Ba2+、Ca2+离子中的一种或两种,因为BaSO4不溶于水,CaSO4微溶于水
(2)Fe(OH)3
(3)AlO2-+CO2+2H2O====Al(OH)3↓+HCO3-
(2)Fe(OH)3
(3)AlO2-+CO2+2H2O====Al(OH)3↓+HCO3-
沉淀A可判断为AgCl,所以Ag+已从溶液中除掉,溶液A中若含Fe2+已被溴水氧化为Fe3+。由于BaSO4难溶于水,CaSO4微溶于水,可判断沉淀B可能是二者之一,也可能是它们的混合物。
Al(OH)3,Fe(OH)3都难溶于水,沉淀C可能是二者之一,或是它们的混合物。若沉淀C中有Al(OH)3,加入过量NaOH溶液后生成NaAlO2进入溶液D,用过量NaOH溶液沉淀C后,仍剩余沉淀D,可判断沉淀D是Fe(OH)3。HAlO2是比H2CO3更弱的酸,其钠盐可被H2CO3沉淀为Al(OH)3,它就是沉淀E。
Al(OH)3,Fe(OH)3都难溶于水,沉淀C可能是二者之一,或是它们的混合物。若沉淀C中有Al(OH)3,加入过量NaOH溶液后生成NaAlO2进入溶液D,用过量NaOH溶液沉淀C后,仍剩余沉淀D,可判断沉淀D是Fe(OH)3。HAlO2是比H2CO3更弱的酸,其钠盐可被H2CO3沉淀为Al(OH)3,它就是沉淀E。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 、Na+等离子的七种溶液一次性鉴别开来的试剂是( )
、Na+等离子的七种溶液一次性鉴别开来的试剂是( )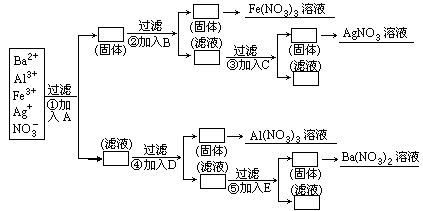
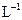 的
的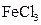 溶液中加入3mL 5mol·
溶液中加入3mL 5mol·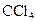 振荡后,静置,不见
振荡后,静置,不见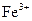 不与
不与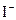 发生反应
发生反应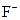 结合成不与
结合成不与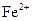 ,使溶液中不再存在
,使溶液中不再存在