��Ŀ����
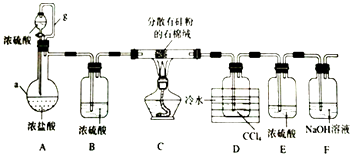
����Ŀ��Ϊ̽����ҵ���ϵ������ã�ij��ѧ��ȤС���������ͼʵ�鷽�����ú�����������ͭ�ĺϽ���ȡ�Ȼ������̷����壨FeSO47H2O���͵������壮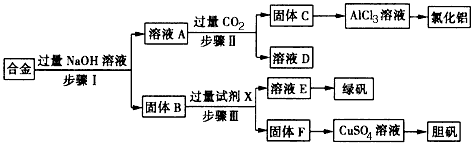
��ش�
��1��������о�����е�ʵ������� �� ʵ�����н��иò���ʱ���õ��IJ����������ձ��� ��
��2����ҺA�е���������Ҫ�����Լ�X�� ��
��3������ҺA��ͨ�����CO2�������ɹ���C�����ӷ���ʽΪ ��
��4���ӻ��������Ƕȿ��ǣ��ù���F�Ʊ�CuSO4��Һ�Ļ�ѧ����ʽ�� ��
���𰸡�
��1�����ˣ���������©��
��2��AlO ![]() ��OH����ϡ����
��OH����ϡ����
��3��AlO ![]() +CO2+H2O�T2Al��OH��3��+HCO
+CO2+H2O�T2Al��OH��3��+HCO ![]()
��4��2Cu+O2+2H2SO4 ![]() 2CuSO4+2H2O
2CuSO4+2H2O
���������⣺��������ͭ�ĺϽ���ֻ�н��������Ժ���������֮�䷴Ӧ������ҺAƫ�����ƣ�����B�ǽ������ͽ���ͭ��A��ͨ������Ķ�����̼���Եõ�������������C��̼��������ҺD�����������Ժ�����֮�䷢����Ӧ�����������������������ǽ���ͭ��ϡ����֮�䲻��Ӧ������������Һ����Ũ������ȴ�ᾧ���Ի���̷����壬����ͭ���Ի�õ������壬��1�������ӹ������������ƣ����������������Ʒ�Ӧ���������ܽ���������ƫ��������Һ���������ͽ���ͭ�����������Ʒ�Ӧ�������Ƿ����ù��ˣ��������˵õ�����Һ�ɷ�Ϊƫ�����ƣ����������ƫ��������ͨ�������Ķ�����̼����õ�����������������������Һ�е�����Ϊ̼�����ƣ������Ƿ����ù��ˣ�������н������ͽ���ͭ�����������Ʒ�Ӧ���������ᷴӦ������ͭ����Ӧ�����Ƿ����ù��ˣ������õ��IJ����������ձ�����������©���ȣ����Դ��ǣ����ˣ���������©������2�������ӹ������������ƣ�������Ӧ����ƫ�����ƺ����������ӷ���ʽΪ2Al+2OH��+2H2O=2AlO ![]() +3H2�����������ͽ���ͭ�����������Ʒ�Ӧ��������ҺA�е�������Ҫ��AlO
+3H2�����������ͽ���ͭ�����������Ʒ�Ӧ��������ҺA�е�������Ҫ��AlO ![]() ��Na+��OH�� �� ���е�������Ϊ��AlO
��Na+��OH�� �� ���е�������Ϊ��AlO ![]() ��OH������ʵ���Ŀ�����ú�����������ͭ�ĺϽ���ȡ�Ȼ������̷����壨FeSO47H2O���͵������壬�������ͽ���ͭ�����������Ʒ�Ӧ���������ᷴӦ������������������ͭ����Ӧ������ʵ�����ֽ����ķ��룬�����Լ�X��ϡ���ᣬ���Դ��ǣ�AlO
��OH������ʵ���Ŀ�����ú�����������ͭ�ĺϽ���ȡ�Ȼ������̷����壨FeSO47H2O���͵������壬�������ͽ���ͭ�����������Ʒ�Ӧ���������ᷴӦ������������������ͭ����Ӧ������ʵ�����ֽ����ķ��룬�����Լ�X��ϡ���ᣬ���Դ��ǣ�AlO ![]() ��OH����ϡ�����3����ҺA�к���ƫ�����ƣ�ƫ��������Һ��ͨ�����CO2����������������������̼�����ƣ���Ӧ�����ӷ���ʽΪ��AlO
��OH����ϡ�����3����ҺA�к���ƫ�����ƣ�ƫ��������Һ��ͨ�����CO2����������������������̼�����ƣ���Ӧ�����ӷ���ʽΪ��AlO ![]() +CO2+H2O�T2Al��OH��3��+HCO
+CO2+H2O�T2Al��OH��3��+HCO ![]() �����Դ��ǣ�AlO
�����Դ��ǣ�AlO ![]() +CO2+H2O�T2Al��OH��3��+HCO
+CO2+H2O�T2Al��OH��3��+HCO ![]() ����4����������ͼ��֪������FΪͭ��ͭ���ܺ�ϡ���ᷴӦ�����ǵ����Ȳ�ͨ�����֮��ͭ��������Ӧ��������ͭ��Ȼ������ͭ������ᷴӦ��������ͭ�����������Ⱦ���������壬����ͭ��Һ����ɫ�ģ����ڸ���Ӧ���ǻ�ϽӴ���һ��ģ���������Ӧ��ͬʱ���еģ���������ͭû���ᵥ���Ĵ��ڣ������ǿ�����Ϊ��Ӧ��Ϊ������ͭ�����ᣬ��������Ϊ����ͭ��ˮ���ʸ÷�Ӧ�Ļ�ѧ����ʽΪ��2Cu+O2+2H2SO4
����4����������ͼ��֪������FΪͭ��ͭ���ܺ�ϡ���ᷴӦ�����ǵ����Ȳ�ͨ�����֮��ͭ��������Ӧ��������ͭ��Ȼ������ͭ������ᷴӦ��������ͭ�����������Ⱦ���������壬����ͭ��Һ����ɫ�ģ����ڸ���Ӧ���ǻ�ϽӴ���һ��ģ���������Ӧ��ͬʱ���еģ���������ͭû���ᵥ���Ĵ��ڣ������ǿ�����Ϊ��Ӧ��Ϊ������ͭ�����ᣬ��������Ϊ����ͭ��ˮ���ʸ÷�Ӧ�Ļ�ѧ����ʽΪ��2Cu+O2+2H2SO4 ![]() 2CuSO4+2H2O�����Դ��ǣ�2Cu+O2+2H2SO4
2CuSO4+2H2O�����Դ��ǣ�2Cu+O2+2H2SO4 ![]() 2CuSO4+2H2O��
2CuSO4+2H2O��

 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�