题目内容
15.下列反应既属于氧化还原反应,又是典型的放热反应的是( )| A. | 铝粉与Fe2O3高温下反应 | B. | Ba(OH)2•8H2O与NH4Cl反应 | ||
| C. | NaOH与H2SO4的中和反应 | D. | 灼热的炭与CO2反应 |
分析 有元素化合价变化的反应,为氧化还原反应;反应物总能量比生成物能量大,则反应为放热反应,结合常见的放热反应来解答.
解答 解:A.反应生成氧化铝和Fe,Al、Fe元素的化合价变化,属于氧化还原反应,且属于放热反应,故A选;
B.没有元素的化合价变化,不属于氧化还原反应,属于吸热反应,故B不选;
C.中和反应中一定没有元素的化合价变化,不属于氧化还原反应,属于放热反应,故C不选;
D.灼热的炭与CO2反应生成CO,C元素的化合价变化,属于氧化还原反应,但为吸热反应,故D不选;
故选A.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析能力和氧化还原反应判断、放热反应判断的考查,题目难度不大.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目
5.银锰精矿是重要的银矿资源,其主要成分为MnO2和银单质,利用黄铁矿(主要成分为FeS2)可以实现锰和银的分离.具体操作流程如图1

(1)提高锰元素浸出率的措施(任写一条)加热或粉碎或充分搅拌等.
(2)浸出1中,黄铁矿转化为铁盐和硫酸盐,请写出发生反应的化学方程式2FeS2+15MnO2+14H2SO4=Fe2(SO4)3+15MnSO4+14H2O.
(3)从工业生产成本考虑,加入的A最好是A.
A.CaCO3 B.NaOH C.氨水 D.Ca(OH)2
(4)浸出液2的主要成分Ag(CN)2-,写出浸出2中发生反应的离子方程式4Ag+O2+8CN-+2H2O=4 Ag(CN)2-+4OH-;电解后的溶液中,可以循环利用的物质NaCN(或CN-)(填化学式).
(5)如图2可知,当液固比(水与矿料的质量比)大于5时,浸出率反而降低的原因NaCN 浓度降低,浸取速率低.
(6)银锰矿中,银矿物以显微粒状分散在MnO2矿物中,不破坏原有结构难以提银,因此锰的浸出对于银的提取率至关重要.某小组通过实验,研究了硫酸用量、黄铁矿用量(占矿重百分比)对锰浸出率的影响,如表所示:
从实际生产角度出发,表中所给浸出条件最佳的是C.

(1)提高锰元素浸出率的措施(任写一条)加热或粉碎或充分搅拌等.
(2)浸出1中,黄铁矿转化为铁盐和硫酸盐,请写出发生反应的化学方程式2FeS2+15MnO2+14H2SO4=Fe2(SO4)3+15MnSO4+14H2O.
(3)从工业生产成本考虑,加入的A最好是A.
A.CaCO3 B.NaOH C.氨水 D.Ca(OH)2
(4)浸出液2的主要成分Ag(CN)2-,写出浸出2中发生反应的离子方程式4Ag+O2+8CN-+2H2O=4 Ag(CN)2-+4OH-;电解后的溶液中,可以循环利用的物质NaCN(或CN-)(填化学式).
(5)如图2可知,当液固比(水与矿料的质量比)大于5时,浸出率反而降低的原因NaCN 浓度降低,浸取速率低.
(6)银锰矿中,银矿物以显微粒状分散在MnO2矿物中,不破坏原有结构难以提银,因此锰的浸出对于银的提取率至关重要.某小组通过实验,研究了硫酸用量、黄铁矿用量(占矿重百分比)对锰浸出率的影响,如表所示:
| 硫酸% | 31.52 | 36.10 | 40.67 | 45.25 |
| 锰浸出率 | 77.42 | 89.49 | 91.59 | 97.95 |
| 黄铁矿% | 12.5 | 15 | 17.5 | 20 |
| 锰浸出率 | 88.79 | 97.95 | 99.18 | 99.46 |
| A | 硫酸45.25% | B | 硫酸31.52% | C | 硫酸45.25% | D | 硫酸36.10% |
| 黄铁矿20% | 黄铁矿15% | 黄铁矿15% | 黄铁矿20% |
6.下列比较错误的是( )
| A. | 稳定性:CH4>SiH4 | B. | 碱性:Mg(OH )2>Ca(OH )2 | ||
| C. | 羟基中H的活泼性:H2O>CH3CH2OH | D. | 原子半径:S>Cl |
3.一定条件下(恒温、恒容的密闭容器中)合成氨反应处于化学平衡状态的是( )
| A. | υ(N2生成)=3υ(H2消耗) | |
| B. | H2、H2、HN3的分子数之比为1:3:2 | |
| C. | 单位时间内生成2molNH3,同时消耗1molH2 | |
| D. | 容器内的压强不再变化 |
10.一种熔融碳酸盐燃料电池原理示意如图.下列有关该电池的说法正确的是( )
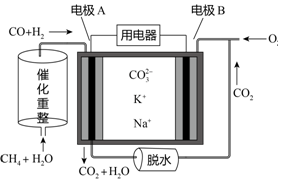

| A. | 电极A上H2和CO都发生了氧化反应 | |
| B. | 反应CH4+H2O$\frac{\underline{\;催化剂\;}}{△}$3H2+CO,每消耗1molCH4转移12mol电子 | |
| C. | 电池工作时,电能转变为化学能 | |
| D. | 电极B上发生的电极反应为:O2+2H2O+4e-═4OH- |
6.在铜锌原电池中,下列叙述正确的是( )
| A. | 正极附近硫酸根离子浓度增大 | |
| B. | 负极附近硫酸根离子浓度增大 | |
| C. | 正负极附近硫酸根离子浓度基本不变 | |
| D. | 若锌片、铜片同时有气泡冒出时,说明锌做正极 |
