题目内容
有五种短周期主族元素A、B、C、D、E,已知:五种元素原子序数依次增大,其中A、E的单质在常温下是气体,B元素原子的最外层电子数是电子层数的2倍,D元素的单质常用于野外焊接铁轨,C元素是所在周期主族元素中原子半径最大的一种。
(1)试写出A、B两种元素形成的不含有非极性键的化合物的电子式: ;
(2)试写出工业上用电解方法冶炼D单质的化学方程式 ;
(3)写出C单质在空气中燃烧的化学方程式,并标出电子转移的方向和数目: ;
(4)写出实验室制取单质E的化学方程式: 。
解析:B元素若为第二周期,则是碳,若为第三周期则是硫,但原子序数比硫大的短周期元素只有氯,故不符合,只能是碳。在野外焊接铁轨用到的单质是Al,故D为铝,又因为A、E的单质在常温下为气体, 则A为氢、E为氯。在同周期主族元素中原子半径最大的是碱金属元素,故C为Na。
答案:(1)![]() (2)2Al2O3
(2)2Al2O3![]() 4Al+3O2 ↑
4Al+3O2 ↑
(3)2Na+O2 Na2O2 (4)MnO2 +4HCl MnCl2 +Cl2↑+2H2O
评注:本题考查的是元素周期律的相关知识,要求考生对元素周期表的结构有清楚的认识和了解。同时本题还考查了化学用语,如电子式的书写、氧化还原反应中电子转移的表示方法等。综合性较强,是一道元素推断题中的好题。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
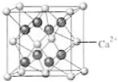 (4)B与Ca形成的晶体的晶胞如右图所示,其中Ca2+的配位数是
(4)B与Ca形成的晶体的晶胞如右图所示,其中Ca2+的配位数是