题目内容
下列是海水综合应用中提取镁、溴的反应,属非氧化还原反应的是
| A.苦卤中加入石灰乳MgCl2+ Ca(OH)2 = CaCl2 +Mg(OH)2 |
| B.苦卤中通入氯气2Br- + Cl2 = 2Cl- + Br2 |
C.氯碱工业电解食盐水2NaCl + 2H2O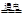 2NaOH + H2↑+ Cl2↑ 2NaOH + H2↑+ Cl2↑ |
D.电解氯化镁MgCl2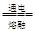 Mg + Cl2↑ Mg + Cl2↑ |
A
解析试题分析:A、MgCl2+ Ca(OH)2 = CaCl2 +Mg(OH)2↓该反应中各元素的化合价均未变,不属于氧化还原反应,正确;B、苦卤中通入氯气,氯、溴元素化合价均发生了变化,属于氧化还原反应,错误;C、氯碱工业电解食盐水氢、氯元素的化合价发生变化,属于氧化还原反应,错误;D、电解氯化镁镁、氯元素的化合价发生变化,属于氧化还原反应 ,错误,答案选A。
考点:考查氧化还原反应的判断

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在加热时,浓硫酸与铜发生反应的化学方程式为:2H2SO4(浓)+Cu  CuSO4+SO2↑+2H2O,对于该反应,下列说法中不正确的是
CuSO4+SO2↑+2H2O,对于该反应,下列说法中不正确的是
| A.是氧化还原反应 | B.浓硫酸是还原剂 |
| C.H2SO4表现了氧化性和酸性 | D.反应中Cu发生了氧化反应 |
某含铬Cr2O72-废水用硫酸亚铁铵[FeSO4·(NH4)2 SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀。该沉淀干燥后得到n molFeO·FeyCrxO3,其中Cr的化合价为+3价。不考虑处理过程中的实际损耗,下列叙述错误的是
| A.消耗硫酸亚铁铵的物质的量为n(2-x)mol |
B.处理废水中Cr2O72- 的物质的量为 mol mol |
| C.反应中转移的电子为3nx mol |
| D.在FeO·FeyCrxO3中3x=y |
科学家最近用金属钠还原CCl4和SiCl4制得一种一维SiC纳米捧。相关反应的化学方程式为:8Na+CCl4十SiCl4=SiC十8NaCl。下列说法不正确的是( )
| A.一维SiC纳米棒“比表面积”大,对微小粒子有较强的吸附能力 |
| B.上述反应中SiC既是氧化产物又是还原产物 |
| C.SiCl4是由极性键构成的非极性分子 |
| D.CCl4分子、SiCl4分子、SiC晶体中各原子都达到了8电子稳定结构 |
三氟化氮(NF3)在微电子工业中有重要用途,可由氨气和氟气反应得到,它在潮湿的空气中与水蒸气反应的产物有HF、NO和HNO3。下列说法错误的是
| A.原子半径:N>F |
| B.在与水蒸气反应中,NF3既是氧化剂又是还原剂 |
| C.若NF3泄漏,可用石灰水溶液喷淋的方法减少污染 |
| D.在潮湿空气中反应,被氧化与被还原的元素的物质的量之比为2:1 |
氧化还原反应与四种基本类型反应的关系如右图所示,则下列化学反应属于4区的是( )。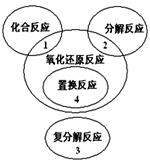
| A.Cl2+2KBr=Br2+2KCl |
| B.2NaHCO3=Na2CO3+H2O+CO2 |
| C.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| D.2Na2O2+2CO2=2Na2CO3+O2 |
在熔融KOH中,大气中的氧可将铬铁矿(FeCr2O4)中Fe和Cr的化合价都转化为+6价,氧化1 mol FeCr2O4在理论上需要氧气( )
| A.2 mol | B.2.5 mol | C.3 mol | D.4 mol |