题目内容
下列说法正确的是( )
| A.N2、CS2、H2O、CH4都是非极性分子 |
| B.SiO2、CsCl、HCl、HF四种晶体的熔点逐渐降低 |
| C.CO2、PCl3、CCl4、CH4四种分子中,各原子都满足最外层8电子结构 |
| D.由原子序数为1和8、1和6的元素,可分别形成原子数之比为1:1的化合物 |
D
选项A中H2O为极性分子。选项B中HF的熔点高于HCl的熔点。选项C中CH4分子中H原子最外层只能达到2电子稳定结构。选项D中H2O2和C2H2都是原子数之比为1:1的化合物。

练习册系列答案
相关题目

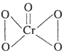 ,据此推断该氧化物
,据此推断该氧化物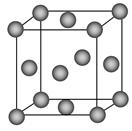
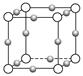
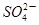 和
和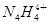 两种离子,当
两种离子,当