题目内容
【题目】已知:(Ⅰ)A是石油裂解气的主要成分,A的产量通常衡量一个国家的石油化工水平。
(Ⅱ)2CH3CHO+O2![]() 2CH3COOH
2CH3COOH
现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
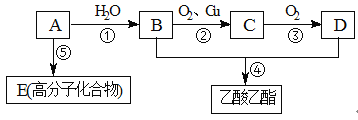
回答下列问题:
(1) 写出A的结构式 。
(2) B、D所含官能团的名称分别是 和 。
(3) 写出下列反应方程式及反应类型:
①方程式 ,反应类型 。
②方程式 ,反应类型 。
【答案】(1) ![]() ;(2) 羟基;羧基 ;
;(2) 羟基;羧基 ;
(3)① CH2=CH2 + H2O![]() CH3CH2OH,加成反应;
CH3CH2OH,加成反应;
② 2CH3CH2OH + O2![]() 2CH3CHO + 2H2O,氧化反应。
2CH3CHO + 2H2O,氧化反应。
【解析】
试题分析:(1)A的产量通常衡量一个国家的石油化工水平,因此A为乙烯,乙烯空间构型为平面形,其结构式为:![]() ;(2)反应①发生加成反应,则B为CH3CH2OH,C为CH3CHO,D为CH3COOH,含有官能团分别是羟基、羧基;(3)反应①发生加成反应,其反应方程式为:CH2=CH2 + H2O
;(2)反应①发生加成反应,则B为CH3CH2OH,C为CH3CHO,D为CH3COOH,含有官能团分别是羟基、羧基;(3)反应①发生加成反应,其反应方程式为:CH2=CH2 + H2O![]() CH3CH2OH,反应②发生醇的氧化,其反应方程式为:2CH3CH2OH + O2
CH3CH2OH,反应②发生醇的氧化,其反应方程式为:2CH3CH2OH + O2![]() 2CH3CHO + 2H2O。
2CH3CHO + 2H2O。

 特高级教师点拨系列答案
特高级教师点拨系列答案【题目】下表为元素周期表前三周期的一部分。
X | Z | ||
W | Y | R | |
(1)X的氢化物的沸点与W的氢化物比较,沸点较高的是:______________(填化学式),原因是_____________________。
(2)从下列选项中选出X的基态原子的最外层原子轨道表示式____________,另一原子轨道表示式不能作为基态原子的轨道表示式是因为它不符合____________。(填序号)。
A. 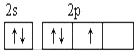 B.
B. 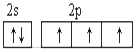
C.泡利原理 D.洪特规则
(3)以上W、Y、R元素原子失去核外第一个电子需要能量由多到少的顺序为:_______________(填元素符号)。
【题目】在2L密闭容器内,800℃时反应:2NO(g)+O2(g)![]() 2NO2(g)体系中,c(NO)随时间的变化如表:
2NO2(g)体系中,c(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)(mol/L) | 0.10 | 0.05 | 0.04 | 0.03 | 0.03 | 0.03 |
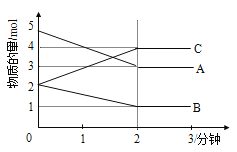
(1)分析上表,该反应达到平衡状态所需时间是_________。
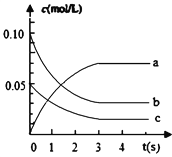
(2)上图中表示NO2的浓度变化曲线是_______________。
(3)用NO表示从0~2s内该反应的平均速率v=________。
(4)v(NO):v(O2) = ______________。
(5)达到平衡状态时O2的转化率为________。