题目内容
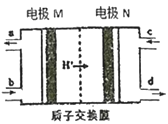
【题目】燃料电池作为安全性能较好的一类化学电源得到了更快的发展,一种以联氨(N2H4)为燃料的环保电池工作原理如图所示,工作时产生稳定无污染的物质。下列说法正确的是
A. M极生成氮气且电极附近pH降低
B. 负极上每消耗1 mol N2H4,会有2 molH+通过质子交换膜
C. 正极的电极反应式为:O2+2H2O+4e-=4OH-
D. 电极M是原电池的正极
【答案】A
【解析】
根据图中氢离子的移动方向可知电极N为正极,电极M为负极,燃料电池中的联氨在负极发生氧化反应,电极反应式为:N2H4-4e-=N2↑+4H+,氧气在正极发生还原反应,电极反应式为:O2+4H++4e-=2H2O。据以上分析进行解答。
根据图中氢离子的移动方向可知电极N为正极,电极M为负极,燃料电池中的联氨在负极发生氧化反应,电极反应式为:N2H4-4e-=N2↑+4H+,氧气在正极发生还原反应,电极反应式为:O2+4H++4e-=2H2O。
A项,结合分析可知电极M为负极,电极反应式为:N2H4-4e-=N2↑+4H+,生成氮气,且会生成H+,导致电极M附近的pH降低,故A项正确;
B项,结合分析可知电极M为负极,联氨在负极发生氧化反应,根据电极反应式可知每消耗 1molN2H4,转移4mol电子,会有4molH+通过质子交换膜,故B项错误;
C项,结合分析可知正极的电极反应式:O2+4H++4e-=2H2O,故C项错误;
D项,根据图中氢离子的移动方向可知电极N为正极,电极M为负极,故D项错误;
正确选项A 。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目